题目内容
实验室用图I所示的装置制取干燥的氨气.
(1)A处反应的化学方程式为
(2)为收集到干燥的氨气,导管C应接
(3)装置B中盛装的试剂的名称是
(4)在水槽中加入水(含酚酞),将充满氨气的试管倒置于放入水槽中(如图Ⅱ所示),将拇指稍移开试管口,可观察到的现象为
(5)在D、E、F三种气体收集方法中,能用于收集NO的是
分析:(1)依据发生装置分析,实验室制备氨气的反应原理是利用固体氯化铵和氢氧化钙固体混合加热反应;
(2)依据收集到干燥的氨气分析,氨气极易溶于水,比空气轻,不能用排水法收集,可以用向下排空气方法收集;
(3)生成的氨气是碱性气体,含有的水蒸气用碱石灰干燥;
(4)依据氨气极易溶于水,和水反应生成一水合氨在溶液中存在电离平衡,是弱碱遇到酚酞变红色;
(5)一氧化氮是比空气略重的气体,难溶于水,易被空气氧化为二氧化氮,依据一氧化氮性质分析判断徐璈收集的装置;
(2)依据收集到干燥的氨气分析,氨气极易溶于水,比空气轻,不能用排水法收集,可以用向下排空气方法收集;
(3)生成的氨气是碱性气体,含有的水蒸气用碱石灰干燥;
(4)依据氨气极易溶于水,和水反应生成一水合氨在溶液中存在电离平衡,是弱碱遇到酚酞变红色;
(5)一氧化氮是比空气略重的气体,难溶于水,易被空气氧化为二氧化氮,依据一氧化氮性质分析判断徐璈收集的装置;
解答:解:(1)实验室制备氨气的反应原理是利用固体氯化铵和氢氧化钙固体混合加热反应,反应的化学方程式为:2NH4Cl+Ca(OH)2
2NH3↑+2H2O+CaCl2;
故答案为:2NH4Cl+Ca(OH)2
2NH3↑+2H2O+CaCl2;
(2)氨气极易溶于水,比空气轻,不能用排水法收集,可以用向下排空气方法收集,选择装置E收集;
故答案为:E;
(3)实验生成的氨气是碱性气体,含有的水蒸气用碱石灰干燥;
故答案为:碱石灰;
(4)氨气极易溶于水溶液进入试管中,和水反应生成一水合氨在溶液中存在电离平衡,电离出氢氧根离子溶液呈碱性,弱碱遇到酚酞变红色;
故答案为:溶液进入试管中,无色溶液变红;
(5)一氧化氮是比空气略重的气体,难溶于水,易被空气氧化为二氧化氮,所以用排水方法收集纯净的一氧化氮气体,所以选择D装置;
故答案为:D;
| ||
故答案为:2NH4Cl+Ca(OH)2
| ||
(2)氨气极易溶于水,比空气轻,不能用排水法收集,可以用向下排空气方法收集,选择装置E收集;
故答案为:E;
(3)实验生成的氨气是碱性气体,含有的水蒸气用碱石灰干燥;
故答案为:碱石灰;
(4)氨气极易溶于水溶液进入试管中,和水反应生成一水合氨在溶液中存在电离平衡,电离出氢氧根离子溶液呈碱性,弱碱遇到酚酞变红色;
故答案为:溶液进入试管中,无色溶液变红;
(5)一氧化氮是比空气略重的气体,难溶于水,易被空气氧化为二氧化氮,所以用排水方法收集纯净的一氧化氮气体,所以选择D装置;
故答案为:D;
点评:本题考查了实验室制备氨气的原理,氨气的性质分析判断,注意氨气极易溶于水生成的一水合氨是弱碱,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 为测定Na3CO3与Na2SO3混合物中各组分的含量,取样品23.2g,用下图所示装置进行实验(铁架台、铁夹等仪器未在图中画出):
为测定Na3CO3与Na2SO3混合物中各组分的含量,取样品23.2g,用下图所示装置进行实验(铁架台、铁夹等仪器未在图中画出): 为测定Na3CO3与Na2SO3混合物中各组分的含量,取样品23.2g,用下图所示装置进行实验(铁架台、铁夹等仪器未在图中画出):
为测定Na3CO3与Na2SO3混合物中各组分的含量,取样品23.2g,用下图所示装置进行实验(铁架台、铁夹等仪器未在图中画出):
 (08上海松江区模拟)乙酸乙酯是重要的工业原料和溶剂。现利用如图
(08上海松江区模拟)乙酸乙酯是重要的工业原料和溶剂。现利用如图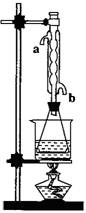 ⑶对于制乙酸乙酯的上述装置,为了提高产率,请提出
⑶对于制乙酸乙酯的上述装置,为了提高产率,请提出