题目内容
12.今有10种物质:①Cu,②.稀硫酸,③HCl,④NH3,⑤空气,⑥CO2,⑦Hg,⑧NaCl,⑨CaCO3,⑩Cl2.按照表中提示的信息,把符合左栏条件的物质的化学式或名称填入右栏相应的位置.| 序号 | 符合的条件 | 物质的化学式或名称 |
| (1) | 混合物 | |
| (2) | 电解质,但熔融状态下并不导电 | |
| (3) | 电解质,但难溶于水 | |
| (4) | 非电解质 | |
| (5) | 既不是电解质,也不是非电解质,但本身能导电 |
分析 (1)混合物中含有两种或两种以上的物质;
(2)电解质是在水溶液或熔化状态下能导电的化合物,酸、弱碱只在水溶液中电离导电;
(3)电解质是在水溶液或熔化状态下能导电的化合物,金属氧化物、部分碱、盐难溶于水,只在熔融状态下导电;
(4)非电解质是在水溶液和熔化状态下都不导电的化合物,并注意电离的物质是否为其本身;
(5)金属单质能导电,溶液能导电,但单质、混合物都既不是电解质,也不是非电解质.
解答 解:(1)稀硫酸是由H2SO4和水组成的混合物;空气中含有氧气、氮气等多种物质属于混合物,
故答案为:稀硫酸、空气;
(2)氯化氢,在水溶液中电离而导电,属于电解质,在熔化状态下只存在氯化氢分子不导电,
故答案为:氯化氢;
(3)碳酸钙固体没有自由移动的离子不导电; 虽然碳酸钙在水中的溶解度很小,难溶于水,只要溶解的部分,就完全电离,碳酸钙在熔融状态下,能完全电离,所以碳酸钙是电解质;
故答案为:碳酸钙;
(4)NH3在水溶液里,生成一水合氨,一水合氨能电离出自由移动的铵根离子和氢氧根离子导致导电,不是氨气自身电离,所以氨气是非电解质,
二氧化碳只存在分子,没有自由移动的离子,所以不能导电;二氧化碳在水溶液中与水反应生成碳酸,碳酸电离出自由移动的离子导电,二氧化碳自身不能电离,二氧化碳是非电解质,
故答案为:NH3、CO2;
(5)铜、汞属于金属单质,能导电,稀硫酸能导电,但属于混合物,则它们既不是电解质,也不是非电解质,
故答案为:Cu、Hg、稀硫酸.
点评 本题考查了物质的分类、电解质、非电解质的概念及导电的原因,明确概念的要点及常见物质的组成或构成是解答的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.用含有少量SiO2(酸性氧化物)的铝片制取纯净的氢氧化铝,有下列操作步骤,最恰当的组合是(按先后顺序排列)( )
①加盐酸溶解
②加过量烧碱溶液溶解
③过滤
④通入过量CO2生成Al(0H)3沉淀
⑤加入盐酸,生成Al(0H)3沉淀
⑥加入过量氨水溶液,生成Al(0H)3沉淀.
①加盐酸溶解
②加过量烧碱溶液溶解
③过滤
④通入过量CO2生成Al(0H)3沉淀
⑤加入盐酸,生成Al(0H)3沉淀
⑥加入过量氨水溶液,生成Al(0H)3沉淀.
| A. | ①③⑥③ | B. | ②③⑥③ | C. | ②③④③ | D. | ②③⑤③ |
7.对于反应H-+NH3═H2+NH2-的正确说法是( )
| A. | 属于置换反应 | B. | H-是氧化剂 | ||
| C. | NH3是还原剂 | D. | 氧化产物和还原产物都是H2 |
17.某烃的一种同分异构体只能生成一氯代物,该烃的分子式不可以是( )
| A. | C3H6 | B. | C5H12 | C. | C6H14 | D. | C8H18 |
4.下列说法正确的是( )
| A. | 已知P(红磷,s)=P(白磷,s)△H>0,则白磷比红磷稳定 | |
| B. | 测定相同物质的量浓度的Na2CO3、Na2SiO3的溶液pH,发现后者的更高,说明碳的非金属性强于硅 | |
| C. | 温度和压强一定时,对于可逆反应:2NO2(g)?N2O4(g),混合气体的密度不再改变,则反应达到平衡状态. | |
| D. | 将NaAlO2溶液与NaHCO3溶液混合后生成白色沉淀,是两种溶液水解相互促进的结果 |
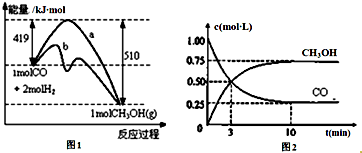 工业上用CO生产燃料甲醇.一定温度和容积条件下发生反应:CO(g)+2H2(g)?CH3OH(g).图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2molH2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化.请回答下列问题:
工业上用CO生产燃料甲醇.一定温度和容积条件下发生反应:CO(g)+2H2(g)?CH3OH(g).图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2molH2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化.请回答下列问题: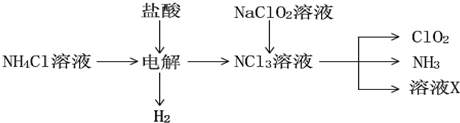
 ,判断下列物质不能与B发生化学反应的有C.
,判断下列物质不能与B发生化学反应的有C.