题目内容
反应A(g)+B(g)  C(g)+D(g)过程中的能量变化如图所示,由此可判断( )
C(g)+D(g)过程中的能量变化如图所示,由此可判断( )
| A.1molA与1molB充分反应后,能量变化为ΔE |
| B.加入催化剂后,反应加快,ΔE减小 |
| C.反应物的总键能小于生成物的总键能 |
| D.反应达到平衡时,升高温度,A的转化率增大 |
D
解析试题分析:A、1molA(g)与1molB(g)充分反应后生成1mol C(g)与1molD(g),能量变化为ΔE,错误;B、加入催化剂后,反应加快,E1、E2减小,ΔE不变,错误;C、由题给图像知,反应物的总键能大于生成物的总键能,错误;D、由题给图像知,该反应为吸热反应,反应达到平衡时,升高温度,平衡正向移动,A的转化率增大,正确。
考点:考查化学反应与能量变化。

练习册系列答案
相关题目
探究NaHCO3、Na2CO3和盐酸(以下盐酸浓度均为1 mol·L-1)反应过程中的热效应,实验测得如下数据:
| 序号 | 35 mL试剂 | 固体 | 混合前 温度/℃ | 混合后 温度/℃ |
| ① | 水 | 2.5 g NaHCO3 | 20.0 | 18.5 |
| ② | 水 | 3.2 g Na2CO3 | 20.0 | 24.3 |
| ③ | 盐酸 | 2.5 g NaHCO3 | 20.0 | 16.2 |
| ④ | 盐酸 | 3.2 g Na2CO3 | 20.0 | 25.1 |
A.Na2CO3溶液与盐酸的反应是吸热反应
B.NaHCO3溶液与盐酸的反应是放热反应
C.20.0 ℃时,含3.2 g Na2CO3的饱和溶液和35 mL盐酸混合后的温度将低于25.1 ℃
D.20.0 ℃时,含2.5 g NaHCO3的饱和溶液和35 mL盐酸混合后的温度将低于16.2 ℃
未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列符合未来新能源标准的是( )
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能
| A.①②③④ | B.⑤⑥⑦⑧ | C.③⑤⑥⑦⑧ | D.③④⑤⑥⑦⑧ |
能将化学能转化为热能的是
| A.光合作用 | B.水力发电 | C.燃煤取暖 | D.燃料电池 |
下列说法正确的是:
A.在100℃、101kPa条件下,液态水的气化热为40. 69 kJ·mol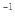 ,则 ,则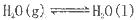  |
B.已知MgCO3的Ksp=6.82×10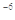 ,则所有含有固体MgCO3的溶液中,都有 ,则所有含有固体MgCO3的溶液中,都有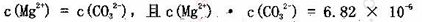 |
C.己知: 则可以计算出反应 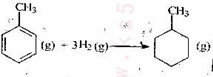  |
D.常温下,在0.10mol 的NH3·H2O溶液中加入少量NH4Cl晶体,能使NH3·H2O的电离度降低,溶液的PH减小 的NH3·H2O溶液中加入少量NH4Cl晶体,能使NH3·H2O的电离度降低,溶液的PH减小 |
一定条件下,发生反应:①M(s)+N(g)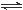 R(g) △H = -Q1 kJ·mol-1,②2R (g)+N(g)
R(g) △H = -Q1 kJ·mol-1,②2R (g)+N(g)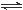 2T (g) △H = -Q2 kJ·mol-1。 Q1、Q2、Q3均为正值。下列说法正确的是
2T (g) △H = -Q2 kJ·mol-1。 Q1、Q2、Q3均为正值。下列说法正确的是
| A.1 mol R(g)的能量总和大于1 mol M(s)与1 mol N(g) 的能量总和 |
| B.将2 mol R (g)与1 mol N(g)在该条件下充分反应,放出热量Q2 kJ |
C.当1 mol M(s)完全转化为T (g)时(假定无热量损失),放出热量Q1+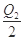 kJ kJ |
D.M(g)+N(g)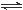 R(g) △H=-Q3 kJ·mol-1 , 则Q3<Q1 R(g) △H=-Q3 kJ·mol-1 , 则Q3<Q1 |
下列反应属于吸热反应的是( )
| A.碳与水蒸气制水煤气的反应 |
| B.生石灰和水的反应 |
| C.盐酸与氢氧化钠溶液的反应 |
| D.木炭在氧气中燃烧 |
下列说法正确的是
| A.物质发生化学变化都伴随着能量变化 |
| B.任何反应中的能量变化都表现为热量变化 |
| C.物质变化时若伴有能量变化,则一定是化学变化 |
| D.没有物质的化学变化,也就没有能量的变化 |
