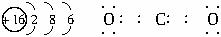题目内容
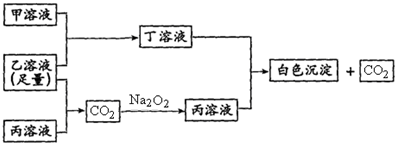
有A、B、C三种常见的短周期单质,A为自然界中最硬的单质,B可与冷、浓硫酸发生钝化,C为淡黄色的固体。甲、乙、丙是3种含氧酸的钠盐,甲中含B元素,乙中含C元素,丙中含A元素,甲、丙溶液pH>7,乙溶液显强酸性;丁为气体,戊为淡黄色固体。甲、乙、丙、丁、戊、己六种物质之间的相互反应关系如下图,请回答: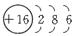
(1)写出C元素的原子结构示意图____________,写出戊的电子式____________;
(2)乙溶液呈强酸性的原因____________(用电离方程式表示);丙溶液呈碱性的原因 ________________________;(用化学反应方程式表示)
(3)写出有关反应的离子方程式
①乙溶液+丙溶液→丁____________________________________;
②己溶液+丙溶液→丁____________________________________。
(1)![]() Na2O2
Na2O2 ![]()
(2)NaHSO4 ![]() Na++H++
Na++H++![]() ,
,
Na2CO3+H2O![]() NaHCO3+NaOH
NaHCO3+NaOH
(3)①2H++![]()
![]() CO2↑+H2O
CO2↑+H2O
② 2Al3++3![]() +3H2O
+3H2O![]() 2Al(OH)3↓+3CO2↑
2Al(OH)3↓+3CO2↑
解析:由题意分析得知:A、B、C分别为碳、铝、硫三元素,甲→己分别是:Na[Al(OH)4](或NaAlO2)。NaHSO4、Na2CO3、CO2、Na2O2、Al2(SO4)3。
(1)S:![]() Na2O2 电子式
Na2O2 电子式![]()
(2)乙呈酸性:![]()
![]() H++
H++![]()
丙呈碱性:Na2CO3+H2O![]() NaHCO3+NaOH
NaHCO3+NaOH
(3)①乙+丙![]() 丁
丁![]() +2H+
+2H+![]() H2O+CO2↑
H2O+CO2↑
②己+丙![]() 丁 3
丁 3![]() +2Al3++3H2O
+2Al3++3H2O![]() 3CO2↑+2Al(OH)3↓
3CO2↑+2Al(OH)3↓

练习册系列答案
相关题目