题目内容
过量的Fe和一定量的稀硝酸完全反应,生成一氧化氮气体1mol,则参加反应的硝酸的物质的量为( )
分析:过量的Fe和一定量的稀硝酸完全反应,发生3Fe+8HNO3═3Fe(NO3)2+2NO↑+4H2O,根据NO的物质的量代入计算.
解答:解:设参加反应的硝酸的物质的量为x,则
3Fe+8HNO3═3Fe(NO3)2+2NO↑+4H2O
8 2
x 1mol
=
,解得x=4mol,
故选C.
3Fe+8HNO3═3Fe(NO3)2+2NO↑+4H2O
8 2
x 1mol
| 8 |
| x |
| 2 |
| 1mol |
故选C.
点评:本题考查学生利用化学反应方程式的计算,明确发生的化学反应是解答本题的关键,难度不大.

练习册系列答案
相关题目

 Fe2(SO4)3 + 3SO2↑+ 6H2O。请你参与探究并回答相关问题。
Fe2(SO4)3 + 3SO2↑+ 6H2O。请你参与探究并回答相关问题。
 Fe2(SO4)3 + 3SO2↑+
6H2O。请你参与探究并回答相关问题。
Fe2(SO4)3 + 3SO2↑+
6H2O。请你参与探究并回答相关问题。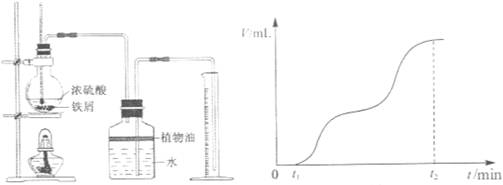
 Fe2(SO4)3
+ 3SO2↑+ 6H2O。请你参与探究并回答相关问题。
Fe2(SO4)3
+ 3SO2↑+ 6H2O。请你参与探究并回答相关问题。