题目内容
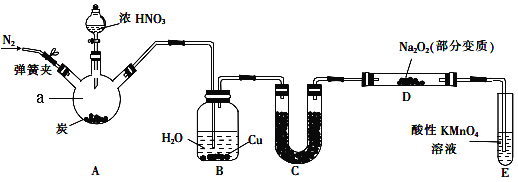
【题目】亚硝酸钠(NaNO2)是一种常见的食品添加剂。某兴趣小组用如图所示装罝制备NaNO2并对其性质作如下探究(A中加热装罝已略去)。
查阅资料可知:
① 2NO+Na2O2![]() 2NaNO2;2NO2+Na2O2
2NaNO2;2NO2+Na2O2![]() 2NaNO3。
2NaNO3。
② NO能被酸性KMnO4氧化成NO3。
(1)装置中仪器a的名称为____________,A中反应的化学方程式是______________________。
(2)装置B中观察到的主要现象是____________________________________________________。
(3)装置C中盛放的试剂是__________________________。
(4)装置E的作用是_______________。
(5)A中滴入浓硝酸之前,应先通入N2一段时间,原因是__________________________________。
(6)写出NO被酸性KMnO4氧化的离子反应方程式_______________________________________。
【答案】 三颈烧瓶(或三颈瓶) C+4HNO3![]() CO2↑+4NO2↑+2H2O 溶液变蓝,铜片溶解,有无色气体冒出 碱石灰(或生石灰或氢氧化钠固体) 吸收有毒气体NO,防止空气污染 排尽装置中的空气,防止对后续实验有干扰 5NO+3MnO4-+4 H+===5NO3+3Mn2+ + 2H2O
CO2↑+4NO2↑+2H2O 溶液变蓝,铜片溶解,有无色气体冒出 碱石灰(或生石灰或氢氧化钠固体) 吸收有毒气体NO,防止空气污染 排尽装置中的空气,防止对后续实验有干扰 5NO+3MnO4-+4 H+===5NO3+3Mn2+ + 2H2O
【解析】(1). 仪器a的名称为三颈烧瓶(或三颈瓶),碳与浓硝酸在加热条件下反应生成CO2、NO2和H2O,化学方程式为:C+4HNO3![]() CO2↑+4NO2↑+2H2O,故答案为:三颈烧瓶(或三颈瓶);C+4HNO3
CO2↑+4NO2↑+2H2O,故答案为:三颈烧瓶(或三颈瓶);C+4HNO3![]() CO2↑+4NO2↑+2H2O;
CO2↑+4NO2↑+2H2O;
(2). B装置中的水和混合气体中的NO2反应生成HNO3和NO,Cu与稀硝酸反应生成Cu(NO3)2、NO和水,所以装置B中观察到的主要现象是:溶液变蓝,铜片溶解,有无色气体冒出,故答案为:溶液变蓝,铜片溶解,有无色气体冒出;
(3). B中得到的NO气体中含有二氧化碳和水蒸气,二氧化碳或水蒸气都能与D装置中的过氧化钠反应,所以为保证制得的亚硝酸钠的纯度,应该除去二氧化碳和水蒸气,所以C中盛放的试剂可以是碱石灰(或生石灰或氢氧化钠固体),故答案为:碱石灰(或生石灰或氢氧化钠固体);
(4). 装置E中盛放的是酸性高锰酸钾溶液,由题中信息可知,酸性高锰酸钾溶液可以吸收多余的有毒气体NO,防止污染空气,故答案为:吸收有毒气体NO,防止空气污染;
(5). 因NO可以和空气中的氧气反应生成二氧化氮,所以A中滴入浓硝酸之前,应先通入N2一段时间,以排尽装置中的空气,防止对后续实验产生干扰,故答案为:排尽装置中的空气,防止对后续实验有干扰;
(6). 由题中信息可知,NO能被酸性KMnO4氧化成NO3,MnO4体现氧化性生成Mn2+,根据得失电子守恒和原子守恒,该反应的离子方程式为:5NO+3MnO4-+4 H+=5NO3+3Mn2+ + 2H2O,故答案为:5NO+3MnO4-+4 H+=5NO3+3Mn2+ + 2H2O。

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案【题目】除去下列物质中的杂质(括号中为杂质),采用的试剂和除杂方法错误的是( )
选项 | 含杂质的物质 | 试剂 | 除杂方法 |
A | C2H4(SO2) | NaOH溶液 | 洗气 |
B | C6H6(苯酚) | 浓Br2水 | 过滤 |
C | C6H5NO2(HNO3) | NaOH溶液 | 分液 |
D | C2H2(H2S) | CuSO4溶液 | 洗气 |
A.A
B.B
C.C
D.D