题目内容
14.现有密度为1.84g•cm-3 98%浓硫酸500mL,其物质的量浓度为多少?分析 根据c=$\frac{1{0}^{3}ρω}{M}$计算该浓硫酸的物质的量浓度,据此分析解答.
解答 解:该浓硫酸的物质的量浓度=$\frac{1000ρω}{M}$=$\frac{1000×1.84×98%}{98}$mol/L=18.4mol/L,
答:该浓硫酸的物质的量浓度为18.4mol/L.
点评 本题考查物质的量浓度有关计算,为高频考点,明确质量分数、物质的量浓度之间关系是解本题关键,注意:物质的量浓度与溶液体积大小无关.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.下列说法中正确的是( )
| A. | 对有气体参加的化学反应,通过减小体积增大体系压强,可使单位体积内活化分子数增加,因而反应速率增大 | |
| B. | 升高温度,主要是因为分子运动加剧,碰撞频率提高,因而反应速率增大 | |
| C. | 活化分子之间发生的碰撞一定为有效碰撞 | |
| D. | 加入适宜的催化剂,可使活化能增大,从而加快反应速率 |
9.下列叙述正确的是( )
| A. | 检验某稀溶液中是否含有NO3-,可先将溶液浓缩,然后加入浓H2SO4和铜片,观察有无红棕色气体产生 | |
| B. | 鉴别NO2和溴蒸气可用AgNO3溶液,也可用湿润的淀粉-KI试纸 | |
| C. | 除去NO中的NO2气体,可通入氧气 | |
| D. | 检验溶液中是否含有NH4+,可加入足量NaOH溶液,加热,再将湿润的红色石蕊试纸伸入试管,观察试纸是否变蓝 |
5. 某校实验室合成环己烯的反应和实验装置(夹持及加热部分已省略)如下:
某校实验室合成环己烯的反应和实验装置(夹持及加热部分已省略)如下:
相关数据如下:
实验步骤:
Ⅰ.[合成]:在a中加入20.00g纯环己醇及2小块沸石,冷却搅动下缓慢加入10mL浓硫酸.b中通入冷却水后,缓慢加热a,控制馏出物的温度不超过90℃.
Ⅱ.[提纯]:将反应后粗产物倒入分液漏斗中,依次用少量5% Na2CO3溶液和水洗涤,分离后加入无水CaCl2颗粒,静置一段时间后弃去CaCl2.再进行蒸馏最终获得12.30g纯环己烯.
回答下列问题:
(1)装置b的名称是直形冷凝管.加入沸石的目的是防止混合液爆沸.
(2)本实验分液所得产物应从上口倒出(填“上口”或“下口”).
(3)提纯过程中加入Na2CO3溶液的目的是除去多余的H2SO4,加入无水CaCl2的作用是干燥所得环己烯(产物).
(4)本实验所得环己烯的产率是75%(产率=$\frac{实际产量}{理论产量}$×100%)
 某校实验室合成环己烯的反应和实验装置(夹持及加热部分已省略)如下:
某校实验室合成环己烯的反应和实验装置(夹持及加热部分已省略)如下:
相关数据如下:
| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解性 | |
| 环已醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环已烯 | 82 | 0.8102 | 83 | 难溶于水 |
Ⅰ.[合成]:在a中加入20.00g纯环己醇及2小块沸石,冷却搅动下缓慢加入10mL浓硫酸.b中通入冷却水后,缓慢加热a,控制馏出物的温度不超过90℃.
Ⅱ.[提纯]:将反应后粗产物倒入分液漏斗中,依次用少量5% Na2CO3溶液和水洗涤,分离后加入无水CaCl2颗粒,静置一段时间后弃去CaCl2.再进行蒸馏最终获得12.30g纯环己烯.
回答下列问题:
(1)装置b的名称是直形冷凝管.加入沸石的目的是防止混合液爆沸.
(2)本实验分液所得产物应从上口倒出(填“上口”或“下口”).
(3)提纯过程中加入Na2CO3溶液的目的是除去多余的H2SO4,加入无水CaCl2的作用是干燥所得环己烯(产物).
(4)本实验所得环己烯的产率是75%(产率=$\frac{实际产量}{理论产量}$×100%)
10.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.请回答下列问题:
(1)常温下,某氨水的pH=12,则水电离的c(OH-)=1×10-12mol/L.若向该氨水中加入等体积、等物质的量浓度的盐酸,此时溶液中水电离的程度大于(填“大于”、“等于”或“小于”)氨水中水的电离程度.
(2)合成氨反应N2(g)+3H2(g)?2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,则平衡向左移动(填“向正反应方向”、“向逆反应方向”或“不”).
(3)一定温度下,在密闭容器中可发生下列反应:2N2O5(g)?4NO2(g)+O2(g).下表为反应在T1温度下的部分实验数据:则500s内N2O5的分解速率v(N2O5)=3×10-3mol•L-1•s-1;降温至T2,反应迸行l000s时测得c(NO2)=4.98mol•L-1,则反应2N2O5(g)?4NO2(g)+O2(g)的△H<0.(填“>”、“=“或“<“).
(4)最近美国Simons等科学家发明了使NH3直接用于燃料电池的方法,其装置用铂黑作电极、加入电解质溶液中,一个电极通人空气,另一电极通入NH3.其电池反应式为:4NH3+3O2=2N2+6H2O.你认为电解质溶液应显碱性(填“酸性”、“中性”或“碱性”),写出正极的电极反应方程式O2+2H2O+4e-=4OH-.
(1)常温下,某氨水的pH=12,则水电离的c(OH-)=1×10-12mol/L.若向该氨水中加入等体积、等物质的量浓度的盐酸,此时溶液中水电离的程度大于(填“大于”、“等于”或“小于”)氨水中水的电离程度.
(2)合成氨反应N2(g)+3H2(g)?2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,则平衡向左移动(填“向正反应方向”、“向逆反应方向”或“不”).
(3)一定温度下,在密闭容器中可发生下列反应:2N2O5(g)?4NO2(g)+O2(g).下表为反应在T1温度下的部分实验数据:则500s内N2O5的分解速率v(N2O5)=3×10-3mol•L-1•s-1;降温至T2,反应迸行l000s时测得c(NO2)=4.98mol•L-1,则反应2N2O5(g)?4NO2(g)+O2(g)的△H<0.(填“>”、“=“或“<“).
| t(秒) | 0 | 500 | 1000 |
| N2O5浓度mol•L-1 | 5.00 | 3.50 | 2.42 |
 气化和液化是使煤变成清洁能源的有效途径,煤的气化的主要反应是C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2,CO和H2的混合气体是合成多种有机物的原料气,研究由CO和H2合成有机物的化学称为一碳化学,如图是合成某些物质的路线图.
气化和液化是使煤变成清洁能源的有效途径,煤的气化的主要反应是C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2,CO和H2的混合气体是合成多种有机物的原料气,研究由CO和H2合成有机物的化学称为一碳化学,如图是合成某些物质的路线图. +2H2O;②A→B:2CH3OH+O2$→_{△}^{Cu}$2HCHO+2H2O.
+2H2O;②A→B:2CH3OH+O2$→_{△}^{Cu}$2HCHO+2H2O.


 ),试写出该两步反应对应的化学方程
),试写出该两步反应对应的化学方程 ;
;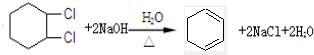 .
.