��Ŀ����
�������������ȵ��ܱ������ж��������·�Ӧ��CO2+H2 CO+H2O,��Ӧ�����¶���ͬ������Ӧ��ʼ��Ũ�Ȳ�ͬ�����У��ף�c��H2��=c��CO2��=amol/L
CO+H2O,��Ӧ�����¶���ͬ������Ӧ��ʼ��Ũ�Ȳ�ͬ�����У��ף�c��H2��=c��CO2��=amol/L
�ң�c��CO2��=amol/L c��H2��="2" amol/L
����c��CO2��=c��H2��=c��H2O��=amol/L
�ﵽƽ��ʱ��һ����̼��Ũ���ɴ�С������ȷ���ǣ� ��
 CO+H2O,��Ӧ�����¶���ͬ������Ӧ��ʼ��Ũ�Ȳ�ͬ�����У��ף�c��H2��=c��CO2��=amol/L
CO+H2O,��Ӧ�����¶���ͬ������Ӧ��ʼ��Ũ�Ȳ�ͬ�����У��ף�c��H2��=c��CO2��=amol/L �ң�c��CO2��=amol/L c��H2��="2" amol/L
����c��CO2��=c��H2��=c��H2O��=amol/L
�ﵽƽ��ʱ��һ����̼��Ũ���ɴ�С������ȷ���ǣ� ��
| A����>��>�� | B����>��>�� | C����>��>�� | D����>��>�� |
D
����������ҿ�����Ϊ���ȼ���c��H2��=c��CO2��=amol/L���ﵽ��ѧƽ��ʱ�ټ���c��H2��=amol/L�����������˷�Ӧ���Ũ�ȣ����Ի�ѧƽ�������ƶ������մﵽƽ��ʱһ����̼��Ũ�ȱȼ״��ڱ�������Ϊ���ȼ���c��H2��=c��CO2��=amol/L���ﵽ��ѧƽ��ʱ�ټ���c��H2O��=amol/L�������������������Ũ�ȣ����Ի�ѧƽ���淴Ӧ�����ƶ������մﵽƽ��ʱһ����̼��Ũ�ȱȼ�С���ﵽƽ��ʱ��һ����̼��Ũ���ɴ�С������ȷ������>��>����ѡ����D��

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
 cZ(g)+dW(g)��Ӧ�ﵽƽ����������ѹ����
cZ(g)+dW(g)��Ӧ�ﵽƽ����������ѹ���� CH3OH(g)
CH3OH(g)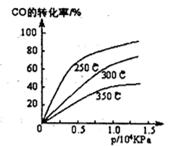
 2NH3��
2NH3��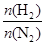 ��ʾ��ʼʱH2��N2�����ʵ���֮�ȣ�����ʼʱH2��N2�����ʵ���֮����ȡ�����ͼ����ȷ����(����)
��ʾ��ʼʱH2��N2�����ʵ���֮�ȣ�����ʼʱH2��N2�����ʵ���֮����ȡ�����ͼ����ȷ����(����)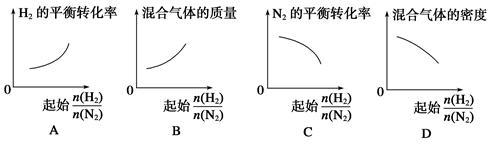
 2 CH3OCOOC2H5(g)������������ͬ��CH3OCOOCH3��ƽ��ת����(��)���¶�(T)����Ӧ����ȣ�R=n(C2H5OCOOC2H5):n(CH3OCOOCH3)���Ĺ�ϵ����ͼ��ʾ�����ַ�Ӧ����ȷֱ�Ϊ1:1��2:1��3:1������˵������ȷ����( )
2 CH3OCOOC2H5(g)������������ͬ��CH3OCOOCH3��ƽ��ת����(��)���¶�(T)����Ӧ����ȣ�R=n(C2H5OCOOC2H5):n(CH3OCOOCH3)���Ĺ�ϵ����ͼ��ʾ�����ַ�Ӧ����ȷֱ�Ϊ1:1��2:1��3:1������˵������ȷ����( )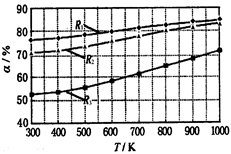
 2NO2��ͨ��18O��ɵ����������´ﵽƽ�����18O
2NO2��ͨ��18O��ɵ����������´ﵽƽ�����18O 2C(g),��Ӧ��ƽ��ʱ�������������A��B�����ʵ���֮����C�����ʵ�����ȣ�����ʱA��ת����Ϊ�� ��
2C(g),��Ӧ��ƽ��ʱ�������������A��B�����ʵ���֮����C�����ʵ�����ȣ�����ʱA��ת����Ϊ�� ��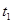 s���ƽ�⡣��ͼ��
s���ƽ�⡣��ͼ��