题目内容
4.下列各组元素各项性质比较正确的是( )| A. | 第一电离能:Li<Be<B | B. | 最高正价:O>N>C | ||
| C. | 电负性:O>C>Si | D. | 半径:K+>Cl- |
分析 A.Be元素最外层为全充满结构,较稳定;
B.F、O无正价;
C.同周期元素从左到右电负性逐渐增大,同主族从上到下电负性逐渐减小;
D.离子核外电子层数相同时,原子序数越大,离子半径越小.
解答 解:A.Be元素最外层为半充满结构,较稳定,应最大,所以第一电离能:Li<B<Be,故A错误;
B.F、O电负性较强,无正价,故B错误;
C.同周期元素从左到右电负性逐渐增大,同主族从上到下电负性逐渐减小,则有电负性:O>C>Si,故C正确;
D.离子核外电子层数相同时,原子序数越大,离子半径越小,半径:K+<Cl-,故D错误.
故选C.
点评 本题考查元素周期律知识,涉及离子半径、电负性、化合价等知识,侧重于学生的分析能力的考查,注意把握周期律的递变规律,学习中注意积累.

练习册系列答案
相关题目
15.某温度下,反应SO2(g)+$\frac{1}{2}$O2(g)═SO3(g) 的平衡常数为K1,在同一温度下,反应2SO3(g)═2SO2(g)+O2(g)的平衡常数为K2,则( )
| A. | K2=K1 | B. | K2=$\frac{1}{{K}_{1}}$ | C. | K2=K${\;}_{1}^{2}$ | D. | K2=$\frac{1}{{K}_{1}^{2}}$ |
12.钛冶炼厂与氯碱厂、甲醇厂组成一个产业链(如图所示),将大大提高资源的利用率,减少环境污染.

请回答下列问题:
(1)Fe位于元素周期表中第四周期,第ⅤⅢ族.
(2)写出钛铁矿在高温下与焦炭经氯化得到四氯化钛的化学方程式2FeTiO3+6C+7Cl2$\frac{\underline{\;高温\;}}{\;}$2FeCl3+2TiCl4+6CO.
(3)制备TiO2的方法之一是利用TiCl4水解生成TiO2•x H2O,再经焙烧制得.水解时需加入大量的水并加热,请结合化学方程式和必要的文字说明原因:发生TiCl4+(2+x)H2O=TiO2•xH2O+4HCl,加入大量水并加热,HCl挥发,促使水解正向进行;
(4)反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于1412℃即可.
(5)用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+.滴定分析时,称取TiO2(摩尔质量为M g/mol)试样w g,消耗c mol/L NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数为$\frac{cVM}{10w}$%.(用代数式表示)
(6)由CO和H2合成甲醇的方程式是:CO(g)+2H2(g)?CH3OH(g).若不考虑生产过程中物质的任何损失,上述产业链中每合成6mol甲醇,至少需额外补充H25mol.

请回答下列问题:
(1)Fe位于元素周期表中第四周期,第ⅤⅢ族.
(2)写出钛铁矿在高温下与焦炭经氯化得到四氯化钛的化学方程式2FeTiO3+6C+7Cl2$\frac{\underline{\;高温\;}}{\;}$2FeCl3+2TiCl4+6CO.
(3)制备TiO2的方法之一是利用TiCl4水解生成TiO2•x H2O,再经焙烧制得.水解时需加入大量的水并加热,请结合化学方程式和必要的文字说明原因:发生TiCl4+(2+x)H2O=TiO2•xH2O+4HCl,加入大量水并加热,HCl挥发,促使水解正向进行;
(4)反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于1412℃即可.
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
(6)由CO和H2合成甲醇的方程式是:CO(g)+2H2(g)?CH3OH(g).若不考虑生产过程中物质的任何损失,上述产业链中每合成6mol甲醇,至少需额外补充H25mol.
19.下列关于反应能量的说法正确的是( )
| A. | Zn(s)+CuSO4(aq)═ZnSO4(aq)+Cu(s)△H=-216 kJ•mol-1,则反应物总能量>生成物总能量 | |
| B. | 相同条件下,如果1 mol氢原子所具有的能量为E1,1 mol氢分子所具有的能量为E2,则2E1=E2 | |
| C. | 101 kPa时,2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1,则H2的燃烧热为571.6 kJ•mol-1 | |
| D. | H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,则含1 mol NaOH的氢氧化钠固体与含0.5 mol H2SO4 的稀硫酸混合后放出57.3 kJ的热量 |
9.下列说法正确的是( )
| A. | 18 g H2O在标准状况下的体积是22.4 L | |
| B. | 22.4 L O2中一定含有6.02×1023个氧分子 | |
| C. | 在标准状况时,20 mL NH3与60 mL N2所含的原子个数比为2:3 | |
| D. | 将80 g NaOH溶于1 L水中,所得溶液中NaOH的物质的量浓度为2 moL/L |
16.关于能源,下列说法错误的是( )
| A. | 能源的开发和利用情况,可以衡量一个国家或地区的科学技术水平 | |
| B. | 目前新能源主要有:煤、石油、天然气、太阳能、氢能、风能等 | |
| C. | 新能源的优点主要是资源丰富、可再生、没有或很少有污染 | |
| D. | 氢能的优点热值高、资源丰富、燃烧产物无污染;缺点是储存和运输困难 |
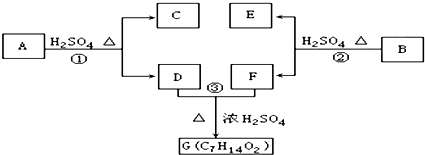
 ;
; ;
; ;写出生成G的化学方程式CH3CH2CH2COOH+
;写出生成G的化学方程式CH3CH2CH2COOH+