题目内容
V L硫酸铝溶液中含有Al3+mg,则溶液中SO42-的物质的量浓度为[ ]
A.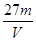 mol/L mol/L | B.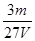 mol/L mol/L | C.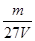 mol/L mol/L | D.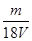 mol/L mol/L |
D
试题分析:mg铝离子的物质的量是
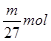 ,则根据硫酸铝的化学式可知,SO42-的物质的量为
,则根据硫酸铝的化学式可知,SO42-的物质的量为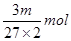 ,所以溶液中SO42-的物质的量浓度为
,所以溶液中SO42-的物质的量浓度为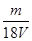 mol/L,答案选D。
mol/L,答案选D。点评:该题是基础性试题的考查,难度不大。该题的关键是判断出两种离子之间的数量关系,然后依据有关的概念直接列式计算即可,有利于培养学生的逻辑推理能力。

练习册系列答案
相关题目
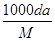
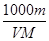
 %
% 与
与 离子总数为0.2NA
离子总数为0.2NA