题目内容
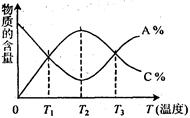
已知可逆反应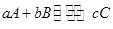 中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是
中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是
A.该反应在T1;T3温度时达到过化学平衡
B.该反应在T2温度时达到过化学平衡
C.该反应的逆反应是放热反应
D.升高温度,平衡会向正反应方向移动
【答案】
B
【解析】
试题分析:选项A、反应在在T1、T3温度时物质A、C的含量相等,当反应速率不相等,故并未达到平衡状态。
选项C、温度由T1到T2变化过程中,反应物A减少,故正反应为放热反应,则其逆反应为吸热反应。
选项D、由图看出,随着反应温度的升高,平衡先正移后逆移。
考点:化学平衡;化学反应与能量;平衡移动
点评:本题主要是对坐标图的分析,属于难度较大的题目。另一方面,需考虑温度对平衡移动的影响,需与反应速率区分。
①对于反应速率,升高温度,正逆反应速率均增大。
②对于平衡移动,升高温度,平衡向吸热反应方向移动。

练习册系列答案
相关题目
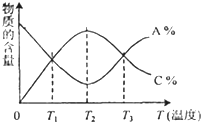 已知可逆反应aA+bB?cC中,物质的含量A%和C%随时间进行、温度的变化曲线如图所示,下列说法正确的是( )
已知可逆反应aA+bB?cC中,物质的含量A%和C%随时间进行、温度的变化曲线如图所示,下列说法正确的是( )| A、该反应在T1温度时已达到过化学平衡 | B、该反应在T3温度时才达到过化学平衡 | C、增大压强平衡一定会向正反应方向移动 | D、该可逆反应的正反应是放热反应 |
已知可逆反应X(g)+Y(g)?Z(g)(未配平).温度为T0时,在容积固定的容器中发生反应各物质的浓度随时间变化的关系如图a所示.其他条件相同,温度分别为T1、T2时发生反应,Z的浓度随时间变化的关系如图b所示.下列叙述正确的是( )
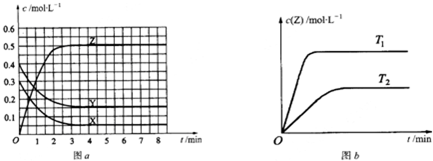

| A、发生反应时,各物质的反应速率大小关系为:v(X)=v(Y)=2v(Z) | B、图a中反应达到平衡时,Y的转化率为37.5% | C、增大压强,平衡向正反应方向移动 | D、该反应正反应的反应热△H>0 |
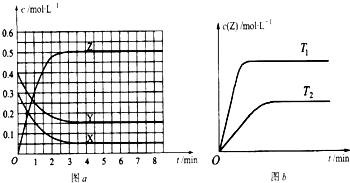 (2009?广州二模)已知可逆反应X(g)+Y(g)?Z(g)(未配平).温度为T0时,在容积固定的容器中发生反应,各物质的浓度随时间变化的关系如图a所示.其他条件相同,温度分别为T1、T2时发生反应,Z的浓度随时间变化的关系如图b所示.下列叙述正确的是( )
(2009?广州二模)已知可逆反应X(g)+Y(g)?Z(g)(未配平).温度为T0时,在容积固定的容器中发生反应,各物质的浓度随时间变化的关系如图a所示.其他条件相同,温度分别为T1、T2时发生反应,Z的浓度随时间变化的关系如图b所示.下列叙述正确的是( )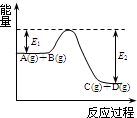 (1)反应A(g)+B(g)
(1)反应A(g)+B(g)  C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
C(g)+D(g)过程中的能量变化如图所示,回答下列问题. P(g)+Q(g)△H>0,请回答下列问题:
P(g)+Q(g)△H>0,请回答下列问题: