题目内容
现有部分短周期元素的性质或原子结构如下表:

(1)元素X的一种同位素可测定文物年代,这种同位素的符号是________(用元素符号表示),元素Z的离子结构示意图为________.
(2)元素Y与氢元素形成一种离子YH![]() 则检测溶液中存在该离子的方法是________________.
则检测溶液中存在该离子的方法是________________.
(3)写出Z元素最高价氧化物对应的水化物与NaOH溶液反应的离子方程式:________.
(4)元素X与元素Y相比,非金属性较强的是________(用元素符号表示),下列表述中证明这一事实的是________.
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物对应的水化物的酸性比X的最高价氧化物对应的水化物的酸性强
c.X与Y形成的化合物中X元素呈正价态
(5)探寻物质的性质差异性是学习的重要方法之一.X、Y、Z三种元素的单质中化学性质明显不同于其他两种单质的是________(用元素符号表示),理由________.
答案:
解析:
解析:
答案:(1)![]() C
C ![]()
(2)向溶液(或待测液)中加入NaOH溶液后加热,能产生使湿润的红色石蕊试纸变蓝的气体,说明溶液中存在该离子,反之,不存在该离子
(3)Al(OH)3+OH-![]() +2H2O
+2H2O
(4)N b、c
(5)Al 具有金属性
解析:根据X元素的核外电子排布特点可知是碳元素;Y的氢化物水溶液显碱性且单质是双原子分子,则Y必是氮元素;Z元素是第三周期简单离子中半径最小的,由于同周期元素的离子半径分成两种情况,阳离子半径依次减小,阴离子半径也是依次减小,但是阴离子半径明显比阳离子半径大很多,因此Z元素必定是第三周期的金属元素铝.其他内容可据题目要求逐一解决.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目


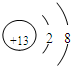




 Al(OH)3
Al(OH)3 Al3++3OH-
Al3++3OH-