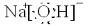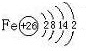ћвƒњƒЏ»Ё
| A£ЃC£®Na+£©£ЊC£®HXO3-£©£ЊC£®OH-£©£ЊC£®H2XO3£©£ЊC£®XO32-£© |
| B£ЃC£®Na+£©+C£®H+£©=C£®OH-£©+C£®XO32-£©+C£®HXO3-£© |
| C£ЃC£®H2XO3£©+C£®HXO3-£©+C£®XO32-£©=C£®Na+£© |
| D£ЃC£®OH-£©=C£®H+£©+C£®HXO3-£©+C£®H2XO3£© |
B£Ѓ”…µзЇ… ЎЇгњ…÷™£ђC£®Na+£©+C£®H+£©=C£®OH-£©+2C£®XO32-£©+C£®HXO3-£©£ђє Bінќу£ї
C£Ѓ”…ќпЅѕ ЎЇгњ…÷™£ђC£®H2XO3£©+C£®HXO3-£©+C£®XO32-£©=C£®Na+£©£ђє C’э»Ј£ї
D£Ѓ”…÷ „” ЎЇгњ…÷™£ђC£®OH-£©=C£®H+£©+C£®HXO3-£©+2C£®H2XO3£©£ђє Dінќу£ї
є —°C£Ѓ

Ѕтћъњу…’‘ь «Ѕтћъњу…ъ≤ъЅтЋбєэ≥ћ÷–≤ъ…ъµƒє§“µЈѕ‘ь£®÷ч“™ЇђFe2O3Љ∞…ўЅњSiO2°ҐAl2O3°ҐCaO°ҐMgOµ»‘”÷ £©°£”√Є√…’‘ь÷∆»°“©”√Є®Ѕѕ°™°™Їм—хїѓћъµƒє§“’Ѕч≥ћ»зѕ¬£Ї
£®1£©‘Џ°∞їє‘≠±Ї…’°±÷–≤ъ…ъµƒ”–ґЊ∆шћењ…ƒ№”– °£
£®2£©°∞Ћбљю°± ±Љд“ї∞г≤ї≥ђєэ20 min£ђ»ф‘Џњ’∆ш÷–Ћбљю ±Љдєэ≥§£ђ»№“Ї÷–Fe2+ЇђЅњљЂѕ¬љµ£ђ∆д‘≠“т”√јл„”Јљ≥ћ љ±н Њ£Ї °£
£®3£©ЄщЊЁѕ¬±н эЊЁ£Ї
| «в—хїѓќп | Al(OH)3 | Mg(OH)2 | Fe(OH)3 | Fe(OH)2 |
| њ™ Љ≥ЅµнµƒpH | 3.10 | 8.54 | 2.01 | 7.11 |
| Ќк»Ђ≥ЅµнµƒpH | 4.77 | 11.04 | 3.68 | 9.61 |
‘Џ°∞≥э‘”°±≤љ÷и÷–£ђќ™≥э»•Fe3+ЇЌAl3+£ђ»№“ЇµƒpH„оіу÷µ”¶–°”Џ £ђµ±pH£љ5 ±£ђ»№“Ї÷–c(Al3+)ќ™ mol°§L£≠1£®“—÷™≥£ќ¬ѕ¬Ksp[Al(OH)3]£љ2.0°Ѕ10£≠33£©°£
£®4£©°∞÷–ЇЌЇѕ≥…°±µƒƒњµƒ «љЂ»№“Ї÷–Fe2+„™±дќ™ћЉЋб—«ћъ≥Ѕµн£ђћЉЋб«впІ”лЅтЋб—«ћъЈі”¶µƒјл„”Јљ≥ћ љќ™ °£
»ф”√µ»ќп÷ µƒЅњµƒћЉЋбпІћжіъћЉЋб«впІ£ђ‘т≤ъ∆Ј÷–њ…ƒ№їм”–µƒ‘”÷ « °£
£®5£©Aµƒ≤ў„ч « °£
£®6£©m g…’‘ьЊ≠єэ…ѕ цє§“’њ…µ√Їм—хїѓћъn g°£“©µд±к„Љєжґ®£ђ÷∆µ√µƒЇм—хїѓћъ÷–Їђ—хїѓћъ≤їµ√…ў”Џ98.0%£ђ‘тЋщ—°”√µƒ…’‘ь÷–ћъµƒ÷ ЅњЈ÷ э”¶≤їµЌ”Џ £®”√Їђm°Ґnµƒ±ніп љ±н Њ£©°£