题目内容
【题目】乙胺是一种一元碱,碱性比一水合氨稍强,在水中电离方程式为![]() 。
。![]() 时,在
时,在![]() 乙胺溶液中滴加
乙胺溶液中滴加![]() 盐酸
盐酸![]() ,混合溶液的
,混合溶液的![]() 与
与 的关系如图所示。下列说法正确的是( )
的关系如图所示。下列说法正确的是( )
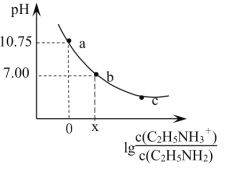
A.在![]() 时加水稀释混合溶液,b点向c点移动
时加水稀释混合溶液,b点向c点移动
B.b点对应溶液中离子浓度关系:![]()
C.在a点时,![]()
D.![]() 时乙胺的电离常数
时乙胺的电离常数![]() 的数量级为
的数量级为![]()
【答案】C
【解析】
乙胺的电离平衡常数为Kb= ,则
,则 ,298K时Kw= c(OH-)·c(H+)=10-14,所以
,298K时Kw= c(OH-)·c(H+)=10-14,所以 =lgKb-pH+14。
=lgKb-pH+14。
A.298K时,pH=7的溶液显中性,加水稀释后仍为中性,即pH不变,所以不移动,故A错误;
B.根据电荷守恒可知![]() ,b点溶液显中性,即c(OH-)=c(H+),所以
,b点溶液显中性,即c(OH-)=c(H+),所以![]() ,但要大于c(OH-)和c(H+),故B错误;
,但要大于c(OH-)和c(H+),故B错误;
C.根据题意,当V=10.00时,溶液中的溶质为等物质的量的C2H5NH2和C2H5NH3Cl,根据 =lgKb-pH+14结合a点坐标可知Kb=10-3.25,则Kh=
=lgKb-pH+14结合a点坐标可知Kb=10-3.25,则Kh=![]() <Kb,所以含有等物质的量的C2H5NH2和C2H5NH3Cl的溶液中C2H5NH2的电离程度较大,即该溶液中c(C2H5NH3+)>c(C2H5NH2),而a点处c(C2H5NH3+)=c(C2H5NH2),所以此时加入的盐酸体积V<10.00,故C正确;
<Kb,所以含有等物质的量的C2H5NH2和C2H5NH3Cl的溶液中C2H5NH2的电离程度较大,即该溶液中c(C2H5NH3+)>c(C2H5NH2),而a点处c(C2H5NH3+)=c(C2H5NH2),所以此时加入的盐酸体积V<10.00,故C正确;
D.a点处 =0,即lgKb-pH+14=0,所以Kb=10-3.25,故D错误;
=0,即lgKb-pH+14=0,所以Kb=10-3.25,故D错误;
故答案为C。

【题目】在相同的密闭容器中,用高纯度纳米级Cu2O分别进行催化分解水的实验:2 H2O(g)![]() 2 H2(g) + O2(g) H>0,实验测得反应体系中水蒸气浓度(mol·L-1)的变化结果如下:
2 H2(g) + O2(g) H>0,实验测得反应体系中水蒸气浓度(mol·L-1)的变化结果如下:
序号 | 时间/min | 0 | 10 | 20 | 30 | 40 | 60 |
① | 温度T1 / 1号Cu2O | 0.0500 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
② | 温度T1 / 2号Cu2O | 0.0500 | 0.0490 | 0.0483 | 0.0480 | 0.0480 | 0.0480 |
③ | 温度T2 / 2号Cu2O | 0.0500 | 0.0480 | 0.0470 | 0.0470 | 0.0470 | 0.0470 |
下列说法不正确的是( )
A. 实验时的温度T2高于T1
B. 2号Cu2O的催化效率比1号Cu2O的催化效率高
C. 实验①前20 min的平均反应速率v(O2) = 7×10ˉ5 mol·Lˉ1·minˉ1
D. 等质量纳米级Cu2O比微米级Cu2O催化效率高,这与Cu2O的粒径大小有关