题目内容
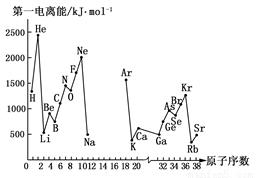
第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量.如图是部分元素原子的第一电离能I1随原子序数变化的曲线图.
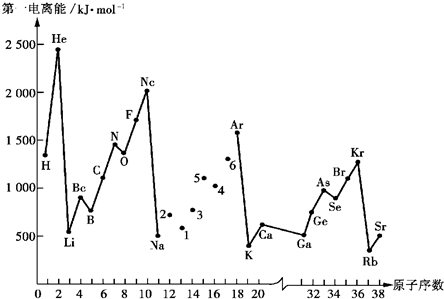
请回答以下问题:
(1)认真分析上图中同周期元素第一电离能的变化规律,将Na--Ar之间六种元素用短线连接起来,构成完整的图象.
(2)从图分析可知,同一主族元素原子的第一电离能I1变化规律是
(3)图中5号元素在周期表中的位置是
(4)图中4、5、6三种元素的电负性大小顺序为

请回答以下问题:
(1)认真分析上图中同周期元素第一电离能的变化规律,将Na--Ar之间六种元素用短线连接起来,构成完整的图象.
(2)从图分析可知,同一主族元素原子的第一电离能I1变化规律是
从上到下依次减小
从上到下依次减小
;(3)图中5号元素在周期表中的位置是
第三周期,ⅤA族
第三周期,ⅤA族
;(4)图中4、5、6三种元素的电负性大小顺序为
6>5>4
6>5>4
.分析:(1)Na--Ar之间六种元素原子序数增加,用短线连接起来再分析第一电离能变化的趋势;
(2)同一主族元素原子的第一电离能I1,从上到下依次减小;
(3)5元素为15号元素氮,在周期表中氮的位置为第三周期,第ⅤA族;
(4)同周期元素从左到右,电负性逐渐增大.
(2)同一主族元素原子的第一电离能I1,从上到下依次减小;
(3)5元素为15号元素氮,在周期表中氮的位置为第三周期,第ⅤA族;
(4)同周期元素从左到右,电负性逐渐增大.
解答:解:(1)Na--Ar之间六种元素原子序数增加,用短线连接起如下图:
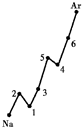 ;
;
故答案为:(1)
 ;
;
(2)同一主族元素原子的第一电离能I1,如上图以第ⅠA族为例,变化规律从上到下依次减小,其他族一致;
故答案为:从上到下依次减小;
(3)5号元素为15号元素氮,在周期表中的位置为第三周期,第ⅤA族;
故答案为:第三周期,ⅤA族;
(4)同周期元素的电负性为从左到右,电负性逐渐增大,即电负性为6>5>4;
故答案为:6>5>4.
 ;
;故答案为:(1)
 ;
;(2)同一主族元素原子的第一电离能I1,如上图以第ⅠA族为例,变化规律从上到下依次减小,其他族一致;
故答案为:从上到下依次减小;
(3)5号元素为15号元素氮,在周期表中的位置为第三周期,第ⅤA族;
故答案为:第三周期,ⅤA族;
(4)同周期元素的电负性为从左到右,电负性逐渐增大,即电负性为6>5>4;
故答案为:6>5>4.
点评:本题考查了第一电离能变化的趋势,同一主族元素原子的第一电离能变化趋势为从上到下依次减小,元素周期表中常见元素的位置,同周期元素从左到右,电负性逐渐增大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量.如图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失).
第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量.如图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失). 主族元素
主族元素 )最近的C(用 表示)的位置.
)最近的C(用 表示)的位置.