题目内容
【题目】在电解液不参与反应的情况下,采用电化学法还原CO2可制备ZnC2O4,原理如图所示。下列说法正确的是

A. 电解结束后电解液Ⅱ中c(Zn2+)增大
B. 电解液Ⅰ应为ZnSO4溶液
C. Pt极反应式为2CO2+2e=![]()
D. 当通入44 g CO2时,溶液中转移1 mol电子
【答案】C
【解析】因为右室Zn失去电子生成Zn2+,溶液中的Zn2+通过阳离子交换膜进入左室,根据电荷守恒,阴离子浓度不变,c(Zn2+)不变,A项错误;右室生成的Zn2+通过阳离子交换膜进入左室与生成的![]()
![]() 结合为ZnC2O4,因此,电解液Ⅰ为稀的ZnC2O4溶液,不含杂质,电解液Ⅱ只要是含Zn2+的易溶盐溶液即可,B项错误;Pt极反应式为2CO2+2e
结合为ZnC2O4,因此,电解液Ⅰ为稀的ZnC2O4溶液,不含杂质,电解液Ⅱ只要是含Zn2+的易溶盐溶液即可,B项错误;Pt极反应式为2CO2+2e![]()
![]() ,C项正确;当通入44 g CO2时,外电路中转移1 mol电子,溶液中不发生电子转移,D项错误。
,C项正确;当通入44 g CO2时,外电路中转移1 mol电子,溶液中不发生电子转移,D项错误。

 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案【题目】下列实验操作对应的现象不符合事实的是
|
|
|
|
A.用铂丝蘸取NaCl溶液置于酒精灯火焰上灼烧,火焰呈黄色 | B.将少量银氨溶液加入盛有淀粉和硫酸的试管中,加热,产生光亮的银镜 | C.饱和食盐水通电一段时间后,湿润的KI-淀粉试纸遇b处气体变蓝色 | D.将胆矾晶体悬挂于盛有浓H2SO4的密闭试管中,蓝色晶体逐渐变为白色 |
A. A B. B C. C D. D
【题目】以天然气代替石油生产液体燃料和基础化学品是当前化学研究和发展的重点。
(1)我国科学家创造性地构建了硅化物晶格限域的单中心铁催化剂,成功实现了甲烷一步高效生产乙烯、芳香烃Y和芳香烃Z等重要化工原料,实现了CO2的零排放,碳原子利用率达100%。已知Y、Z的相对分子质量分别为78、128,其一氯代物分别有1种和2种。
①有关化学键键能数据如表中所示:
化学键 | H-H | C=C | C-C | C≡C | C-H |
E(kJ/mol) | 436 | 615 | 347.7 | 812 | 413.4 |
写出甲烷一步生成乙烯的热化学方程式:_____________;
②已知:原子利用率=期望产物总质量/反应物总质量×100%,则甲烷生成芳香烃Y的原子利用率为______;
③生成1 mol Z产生的H2约合标准状况下________L。
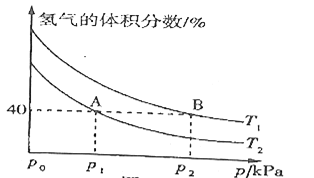
(2)如图为乙烯气相直接水合法制备乙醇过程中乙烯的平衡转化率与温度、压强的关系[其中n(H2O)∶n(C2H4)=1∶1]。
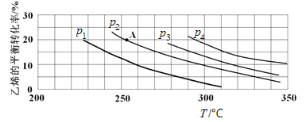
①若p2=8.0 MPa,列式计算A点的平衡常数Kp=_______(用平衡分压代替平衡浓度计算;分压=总压×物质的量分数;结果保留到小数点后两位);
②该反应为______(填“吸热”或“放热”)反应,图中压强(p1、p2、p3、p4)的大小关系为_______;