题目内容
全钒液流电池是一种新型的绿色环保储能电池,该电池性能优良,其电池总反应为:v3++VO2++H2O
VO2++2H++V2+.下列叙述正确的是( )
| 充电 |
| 放电 |
分析:根据电池总反应和参加物质的化合价的变化可知,反应中V2+离子被氧化,应是电源的负极,VO2+离子化合价降低,被还原,应是电源的正极反应,根据原电池的工作原理进行分析,
A.根据阳极上发生的电极反应式判断酸性变化;
B.充电时,阳极上得电子发生还原反应;
C.放电过程中,电解质溶液中的阳离子向正极移动;
D.放电时,根据 V2+与转移电子之间的关系式判断.
A.根据阳极上发生的电极反应式判断酸性变化;
B.充电时,阳极上得电子发生还原反应;
C.放电过程中,电解质溶液中的阳离子向正极移动;
D.放电时,根据 V2+与转移电子之间的关系式判断.
解答:解:A.充电时,阳极反应式为:VO2++H2O=VO2++2H++e-,所以阳极附近溶液的酸性增强,故A错误;
B.充电时,阳极反应式为:VO2++H2O=VO2++2H++e-,故B错误;
C.放电时,该装置是原电池,电解质溶液中的阳离子向正极移动,阴离子向负极移动,故C错误;
D.放电时,负极上V2+被氧化生成v3+,每转移1mol电子,负极有1mol V2+被氧化,故D正确;
故选D.
B.充电时,阳极反应式为:VO2++H2O=VO2++2H++e-,故B错误;
C.放电时,该装置是原电池,电解质溶液中的阳离子向正极移动,阴离子向负极移动,故C错误;
D.放电时,负极上V2+被氧化生成v3+,每转移1mol电子,负极有1mol V2+被氧化,故D正确;
故选D.
点评:本题考查原电池的工作原理,题目难度不大,注意把握原电池中电子及溶液中离子的定向移动问题,本题从化合价的变化进行判断是做题的关键.

练习册系列答案
相关题目
以下是对化学反应变化过程及结果的研究。按要求回答问题:
Ⅰ.关于反应速率和限度的研究
(1)已知25℃时有关弱酸的电离平衡常数:
弱酸化学式 | CH3COOH | HCN | H2CO3 |
电离平衡常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
则等物质的量浓度的①CH3COONa、②NaCN、③Na2CO3、④NaHCO3溶液的pH由大到小的顺序为__________(填编号)。
(2)已知2SO2(g)+O2(g)??2SO3(g) ΔH=-196.6 kJ·mol-1,在一个容积为2 L的容器中加入2 mol SO2和1 mol O2,在某温度下充分反应,经过30 min达到平衡,放出热量176.94 kJ。如果用SO2表示该反应的反应速率,则v(SO2)=________。
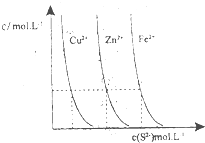
(3)下图为某温度下,CuS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液的S2-浓度、金属阳离子浓度变化情况。如果向三种沉淀中加盐酸,最先溶解的是________。

向新生成的ZnS浊液中滴入足量含相同浓度的Cu2+、Fe2+的溶液,振荡后,ZnS沉淀会转化为________(填化学式)沉淀。
Ⅱ.关于电化学的研究
全钒液流电池是一种新型的绿色环保储能电池。其电池总反应为:VO2++2H++V2+ V3++VO2++H2O。则充电时阳极反应式为__________________________,用此电池电解1 L 1 mol·L-1的CuSO4溶液,当转移0.1 mol电子时,溶液的pH=________(不考虑溶液体积变化)。
V3++VO2++H2O。则充电时阳极反应式为__________________________,用此电池电解1 L 1 mol·L-1的CuSO4溶液,当转移0.1 mol电子时,溶液的pH=________(不考虑溶液体积变化)。
 以下是对化学反应变化过程及结果的研究.按要求回答问题:
以下是对化学反应变化过程及结果的研究.按要求回答问题:

 VO2++H2O+V3+,电池放电时正极的电极反应式为___________。
VO2++H2O+V3+,电池放电时正极的电极反应式为___________。