题目内容
12g Mg与足量的稀盐酸混合,充分反应后得到200ml溶液,求生成MgCl2的物质的量浓度为多少?标准状况下最多能收集到多少升气体?
考点:化学方程式的有关计算
专题:计算题
分析:发生反应Mg+2HCl═MgCl2+H2↑,根据n=
计算12g Mg的物质的量,根据方程式计算生成MgCl2的物质的量、生成氢气的物质的量,再根据c=
计算氯化镁浓度,根据V=nVm计算氢气的体积.
| m |
| M |
| n |
| V |
解答:
解:12g Mg的物质的量=
=0.5mol
Mg+2HCl═MgCl2+H2↑
1 1 1
0.5mol n(FeCl2) n(H2)
n(MgCl2)=
=0.5mol,
n(H2)=
=0.5mol,
故c(MgCl2)=
=2.5mol/L,
V(H2)=0.5mol×22.4L/mol=11.2L,
答:生成MgCl2的物质的量浓度为2.5mol/L;标准状况下最多能收集到11.2L气体.
| 12g |
| 24g/mol |
Mg+2HCl═MgCl2+H2↑
1 1 1
0.5mol n(FeCl2) n(H2)
n(MgCl2)=
| 0.5mol×1 |
| 1 |
n(H2)=
| 0.5mol×1 |
| 1 |
故c(MgCl2)=
| 0.5mol |
| 0.2L |
V(H2)=0.5mol×22.4L/mol=11.2L,
答:生成MgCl2的物质的量浓度为2.5mol/L;标准状况下最多能收集到11.2L气体.
点评:本题考查根据方程式进行的计算,比较基础,注意理解方程式表示的意义,注意根据方程式计算左右单位不一致时,应左右单位相当、上下单位一致.

练习册系列答案
相关题目
在0.1mol?L-1 CH3COOH溶液中存在电离平衡CH3COOH?CH3COO-+H+,当加入下列物质时可使其电离程度和pH都减小的是( )
| A、CH3COONa浓溶液 |
| B、NH3?H2O |
| C、浓盐酸 |
| D、H2O |
某CuSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,已知溶液中阳离子的浓度相等(不考虑水解),且SO42-的物质的量浓度为9mol/L,则此溶液最多溶解Mg的质量为( )
| A、24g | B、18g |
| C、21.6g | D、14.4g |
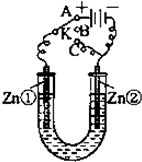 在一个U形管里盛有氯化铜溶液,并插入两块纯锌片作电极,如图所示:
在一个U形管里盛有氯化铜溶液,并插入两块纯锌片作电极,如图所示: