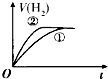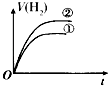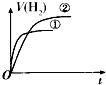题目内容
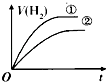
【题目】对于可逆反应A(g)+2B(g)2C(g)(正反应吸热),下列图象正确的是( )
A.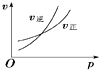
B.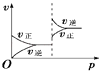
C.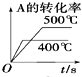
D.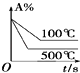
【答案】D
【解析】解:A.该反应为吸热反应,升高温度化学平衡应正向移动,正反应速率大于逆反应速率,但图象中取交点后的某点可知逆反应速率大于正反应速率,故A错误;B.增大压强,化学平衡正向移动,重新达到平衡后正反应速率大于逆反应速率,与图象不符,故B错误;
C.温度高,反应速率大,先到达平衡,即500℃时先达到平衡状态,与图象不符,故C错误;
D.由图象可知,温度高的先达到平衡,且温度高时向正反应进行的程度大,则A的含量低,故D正确;
故选D.
可逆反应A(g)+2B(g)2C(g)(正反应吸热),则升高温度,正逆反应速率均增大,化学平衡正向移动;增大压强,化学平衡正向移动,结合图象来解答.

练习册系列答案
相关题目