题目内容
下列各组物质相互混合后,不会发生离子反应的是( )
| A、NaOH溶液和稀H2SO4 |
| B、KNO3溶液和NaCl溶液 |
| C、Na2CO3溶液和CaCl2溶液 |
| D、Zn和盐酸 |
考点:离子反应发生的条件
专题:离子反应专题
分析:A.氢氧根离子与氢离子反应生成水;
B.KNO3溶液和NaCl溶液不反应;
C.碳酸根离子与钙离子反应生成碳酸钙沉淀;
D.锌与氢离子反应生成锌离子和氢气.
B.KNO3溶液和NaCl溶液不反应;
C.碳酸根离子与钙离子反应生成碳酸钙沉淀;
D.锌与氢离子反应生成锌离子和氢气.
解答:
解:A.NaOH溶液和稀H2SO4发生复分解反应,氢氧根离子与氢离子反应生成水,故A不选;
B.KNO3溶液和NaCl溶液不反应,故B选;
C.Na2CO3溶液和CaCl2溶液发生复分解反应,碳酸根离子与钙离子反应生成碳酸钙沉淀,故C不选;
D.Zn和盐酸发生置换反应,锌与氢离子反应生成锌离子和氢气,故D不选,
故选B.
B.KNO3溶液和NaCl溶液不反应,故B选;
C.Na2CO3溶液和CaCl2溶液发生复分解反应,碳酸根离子与钙离子反应生成碳酸钙沉淀,故C不选;
D.Zn和盐酸发生置换反应,锌与氢离子反应生成锌离子和氢气,故D不选,
故选B.
点评:本题考查离子反应的有关知识,难度不大.要注意发生离子反应的条件是解题的关键.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
有关CH2=CH-C≡N分子的说法正确的是( )
| A、3个σ键,3个π键 |
| B、4个σ键,3个2π键 |
| C、6个σ键,2个π键 |
| D、6个σ键,3个π键 |
对制冷剂氟利昂-12(CF2Cl2)的叙述正确的是( )
| A、只有一种结构 |
| B、有两种结构 |
| C、有四种不同的结构 |
| D、无法确定其结构 |
现有A、B、C、D四种金属片:
①把A、B用导线连接后同时浸入稀硫酸中,B表面变黑并逐渐溶解;
②把C、D用导线连接后同时浸入稀硫酸中,C发生氧化反应;
③把A、C用导线连接后同时浸入稀硫酸中,电子流动方向为A→导线→C.
根据上述情况,下列说法中正确的是( )
①把A、B用导线连接后同时浸入稀硫酸中,B表面变黑并逐渐溶解;
②把C、D用导线连接后同时浸入稀硫酸中,C发生氧化反应;
③把A、C用导线连接后同时浸入稀硫酸中,电子流动方向为A→导线→C.
根据上述情况,下列说法中正确的是( )
| A、在①中,金属片B发生还原反应 |
| B、在②中,金属片C作正极 |
| C、如果把B、D用导线连接后同时浸入稀硫酸中,则金属片D上有气泡产生 |
| D、上述四种金属的活动性由强到弱的顺序是:A>B>C>D |
下列微粒的核外电子排布错误的是( )
A、 |
B、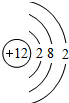 |
C、 |
D、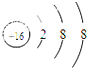 |
X、Y为同主族元素,Y的原子半径大于X.下列说法正确的是(m、n均为正整数)( )
| A、若X(OH)n为强碱,则Y(OH)n也一定为强碱 |
| B、若HnXOm为强酸,则X的氢化物溶于水一定显酸性 |
| C、若HnY的水溶液为酸性,则HnX的酸性比HnY的酸性更强 |
| D、若Y的最高正价为+7,则X的最高正价一定为+7 |
下列各组中每种物质都既有离子键又有共价键的一组是( )
| A、NaOH、H2SO4、(NH4)2SO4 |
| B、MgO、Na2SO4、HNO3 |
| C、Na2O2、KOH、Na3PO4 |
| D、HCl、Fe2O3、MgCl2 |
下列热化学方程式或说法正确的是( )
| A、甲烷的燃烧热为△H=-890kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890 kJ?mol-1 | |||
| B、500℃、30MPa下,将0.5mol N2和1.5mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为: N2(g)+3H2(g)
| |||
| C、已知:H2(g)+F2(g)=2HF(g);△H=-270 kJ/mol,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ | |||
| D、在C中相同条件下,2 mol HF气体的能量小于1 mol氢气与1 mol氟气的能量总和 |