��Ŀ����
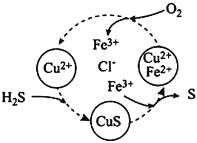
����Ŀ��ij��ѧ��ȤС��Ϊ��̽��ԭ��ز��������Ĺ��̣��������ͼ��ʾʵ�飺
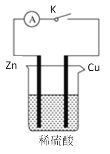
��1��������������ȷ����___��
A.����KʱͭƬ���������رտ���KʱͭƬ������
B.����K��пƬ��ͭƬ�Ͼ������ݲ���
C.�رտ���K����Һ�е�H��Ũ�ȼ�С
D.�رտ���K�������ݵ����ʱȴ���Kʱ��
��2������K��װ���з�����Ӧ�����ӷ���ʽΪ___��
��3���رտ���K�����װ��Ϊ___(����ԭ���������������)��п��Ϊ___��(��������������������������������)��ͭ���ϵĵ缫��ӦʽΪ__������Ӧ��������0.3mol�ĵ��ӷ���ת�ƣ�������������ڱ�״���µ����Ϊ___L��
���𰸡�C Zn+2H��=Zn2++H2�� ԭ��� �� 2H����2e-=H2�� 3.36
��������
����ϵ�з�����ӦZn+H2SO4=ZnSO4+H2����������K�պ�ʱ���γɱպϻ�·����ԭ��أ���ʱZn�缫����������ӦΪ������Cu�缫Ϊ����������K�������γɱպϻ�·����ʱZn�缫�Ϸ����û���Ӧ��
(1)A������K���γɱպϻ�·�������γ�ԭ��أ���A����
B������K��ֻ��Zn��ϡ���ᷢ���û���Ӧ���������ݣ�ͭ�缫������������B����
C���رտ���K���γ�ԭ��أ�����ܷ�ӦΪZn+H2SO4=ZnSO4+H2������Һ�е�H��Ũ�ȼ�С����C��ȷ��
D���رտ���K���γ�ԭ��أ�ԭ��ؿ��Լӿ�������ԭ��Ӧ���ʣ���D����
��������ѡC��
(2)��K��Zn��ϡ���ᷢ���û���Ӧ�����ӷ���ʽΪZn+2H��=Zn2++H2����
(3)�ر�K��װ��Ϊԭ���װ�ã�п������������ӦΪ������ͭ�缫Ϊ�����������ܷ�Ӧ�ɵ�ͭ�缫�ķ�ӦΪ2H����2e-=H2����ת��0.3mol����ʱ������������0.15mol����������Ϊ3.36L��

����Ŀ����ҵ�������ڽӴ����з�������Ҫ��ӦΪ2SO2(g)��O2(g)![]() 2SO3(g)����һ���¶��£���2L�ܱ�������Ͷ��4molSO2(g)��2molO2(g)����������Ӧ��n(SO2)��ʱ��ı仯�����ʾ��
2SO3(g)����һ���¶��£���2L�ܱ�������Ͷ��4molSO2(g)��2molO2(g)����������Ӧ��n(SO2)��ʱ��ı仯�����ʾ��
ʱ��(s) | 0 | 1 | 2 | 3 | 5 |
n(SO2)(mol) | 4 | 3.2 | 1.6 | 1.4 | 1.4 |
��1����SO3��ʾ��0~2s�ڸ÷�Ӧ��ƽ������v(SO3)=___��
��2���÷�Ӧ�ﵽ�����ʱSO2��ת����Ϊ___��
(��ʾ��ת����=![]() ��100%)
��100%)
��3���÷�Ӧ�ﵽ�����ʱO2��Ũ��Ϊ___��
��4������������˵��������Ӧ�ﵽƽ��״̬����___��
A.������ѹǿ���ֲ���
B.v��SO2��=2v(O2)
C.SO3��Ũ�Ȳ��ٱ仯
D.SO2��O2��SO3ΪŨ��֮��Ϊ2��1��2
E.��λʱ����ÿ����2molSO2��ͬʱ����2molSO3