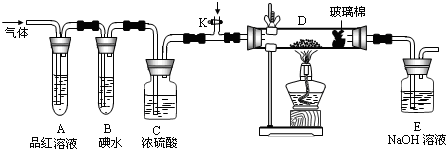
题目内容
在氯化钡溶液中通入二氧化硫气体,溶液澄清;若将氯化钡溶液分盛两支试管,一支加硝酸,另一支加烧碱溶液,然后再通入二氧化硫气体,结果两支试管都有白色沉淀生成。由此得出下列结论合理的是( )A.两支试管中的沉淀均是亚硫酸钡
B.二氧化硫既有还原性,又具有酸性氧化物的性质
C.BaCl2有两性
D.pH升高或降低均能使二氧化硫水溶液中的![]() 浓度增大而产生沉淀
浓度增大而产生沉淀
B
解析:若氯化钡与二氧化硫能反应,反应的产物必为亚硫酸钡和盐酸,而盐酸和亚硫酸钡不能共存,所以反应不能发生。当加入硝酸时,3SO2+2HNO3+2H2O====3H2SO4+2NO,H2SO4+BaCl2====BaSO4↓+2HCl;当加入烧碱时,SO2+2NaOH====Na2SO3+H2O,Na2SO3+BaCl2====BaSO3↓+2NaCl。在加硝酸时,二氧化硫表现出还原性;在加烧碱时,二氧化硫表现出酸性氧化物的性质。在二氧化硫水溶液中,加入烧碱,使其pH增大,此时溶液中的![]() 浓度增大;加酸时,pH降低,此时酸的存在将抑制亚硫酸的电离,从而使溶液中的
浓度增大;加酸时,pH降低,此时酸的存在将抑制亚硫酸的电离,从而使溶液中的![]() 浓度减小。
浓度减小。

练习册系列答案
相关题目
 Na2SO4+SO2↑+H2O(注:80%H2SO4具有浓硫酸的特性)
Na2SO4+SO2↑+H2O(注:80%H2SO4具有浓硫酸的特性)


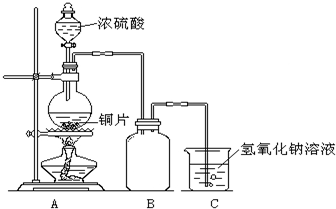 某化学课外兴趣小组为探究铜与浓硫酸的反应,用右图所示的装置进行实验:
某化学课外兴趣小组为探究铜与浓硫酸的反应,用右图所示的装置进行实验: