题目内容
X、Y和W为原子序数依次递增的短周期元素.已知:X和Y同主族,Y和W的氢化物具有相同的电子数.在中学范围内X的单质只有氧化性,且是空气的主要成份之一.
(1)写出实验室制取W2反应的离子方程式 .
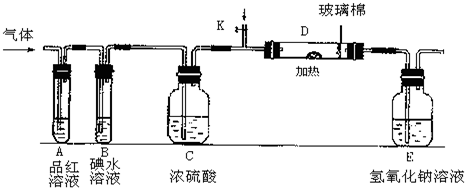
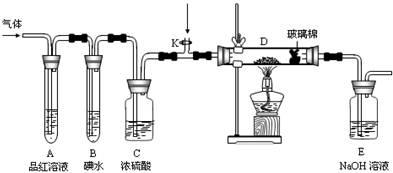
(2)某小组设计如图所示的装置,分别研究YX2和W2的性质.
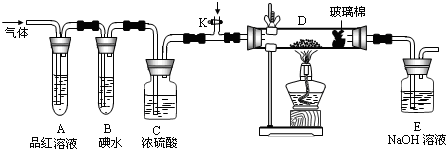
①分别通入YX2和W2,在装置A中观察到的现象是否相同 (填“相同”或“不相同”);若装置D中装的是铜粉,当通入足量W2时观察到的现象为 ;若装置D中装的是五氧化二钒(催化剂),当通入足量YX2时,打开K通入适量X2,化学反应方程式为 .
②若装置B中装有5.0mL 1.0×10-3mol/L的碘水,当通入足量W2完全反应后,转移了5.0×10-5mol电子,该反应的化学方程式为 .
(3)某同学将足量的YX2通入一支装有氯化钡溶液的试管,未见沉淀生成,再向该试管中加入过量的下列溶液也无沉淀生成的是 (填字母).
A.氨水 B.稀盐酸 C.稀硝酸 D.氯化钙 E.双氧水 F.硝酸银.
(1)写出实验室制取W2反应的离子方程式
(2)某小组设计如图所示的装置,分别研究YX2和W2的性质.

①分别通入YX2和W2,在装置A中观察到的现象是否相同
②若装置B中装有5.0mL 1.0×10-3mol/L的碘水,当通入足量W2完全反应后,转移了5.0×10-5mol电子,该反应的化学方程式为
(3)某同学将足量的YX2通入一支装有氯化钡溶液的试管,未见沉淀生成,再向该试管中加入过量的下列溶液也无沉淀生成的是
A.氨水 B.稀盐酸 C.稀硝酸 D.氯化钙 E.双氧水 F.硝酸银.
分析:X、Y和W为原子序数依次增大的短周期元素,中学范围内X的单质只有氧化性,且是空气的主要成份之一,则X为O元素;X和Y同主族,则Y为S元素;Y和W的氢化物具有相同的电子数,氢化物电子数为18,结合原子序数可知W为Cl元素,
(1)实验室常用二氧化锰与浓盐酸反应准备氯气,反应生成氯化锰、氯气与水;
(2)①二氧化硫与品红化合为无色物质,氯气与水反应生成次氯酸,次氯酸具有强氧化性,将品红氧化为无色物质;氯气与铜反应产生棕黄色的烟;二氧化硫在五氧化二钒作催化剂、加热条件下与氧气反应生成三氧化硫;
②令碘元素在氧化产物中的化合价为a,则根据电子转移守恒有5.0×10-3L×1.0×10-3mol/L×2×a=5.0×10-5mol,解得a=+5,所以碘单质被氧化为HIO3,据此书写方程式;
(4)二氧化硫溶于水,呈酸性,且具有还原性,故碱性物质能与二氧化硫在溶液在生成亚硫酸盐、强氧化性物质可以将二氧化硫氧化为硫酸,能与氯化钡反应生成亚硫酸钡、硫酸钡沉淀,硝酸银溶液与氯化钡溶液生成AgCl白色沉淀,据此解答.
(1)实验室常用二氧化锰与浓盐酸反应准备氯气,反应生成氯化锰、氯气与水;
(2)①二氧化硫与品红化合为无色物质,氯气与水反应生成次氯酸,次氯酸具有强氧化性,将品红氧化为无色物质;氯气与铜反应产生棕黄色的烟;二氧化硫在五氧化二钒作催化剂、加热条件下与氧气反应生成三氧化硫;
②令碘元素在氧化产物中的化合价为a,则根据电子转移守恒有5.0×10-3L×1.0×10-3mol/L×2×a=5.0×10-5mol,解得a=+5,所以碘单质被氧化为HIO3,据此书写方程式;
(4)二氧化硫溶于水,呈酸性,且具有还原性,故碱性物质能与二氧化硫在溶液在生成亚硫酸盐、强氧化性物质可以将二氧化硫氧化为硫酸,能与氯化钡反应生成亚硫酸钡、硫酸钡沉淀,硝酸银溶液与氯化钡溶液生成AgCl白色沉淀,据此解答.
解答:解:X、Y和W为原子序数依次增大的短周期元素,中学范围内X的单质只有氧化性,且是空气的主要成份之一,则X为O元素;X和Y同主族,则Y为S元素;Y和W的氢化物具有相同的电子数,氢化物电子数为18,结合原子序数可知W为Cl元素,
(1)实验室常用二氧化锰与浓盐酸反应准备氯气,反应生成氯化锰、氯气与水,反应离子方程式为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,
故答案为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O;
(2)①二氧化硫与品红化合物无色物质,氯气与水反应生成次氯酸,次氯酸具有强氧化性,将品红氧化为无色物质,二氧化硫与氯气都可以是品红溶液褪色,在装置A中观察到的现象是相同;氯气与铜反应产生棕黄色的烟;二氧化硫在五氧化二钒作催化剂、加热条件下与氧气反应生成三氧化硫,反应方程式为:2SO2+O2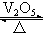 2SO3
2SO3
故答案为:相同;产生棕黄色的烟;2SO2+O2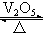 2SO3;
2SO3;
②若装置B中装有5.0mL 1.0×10-3mol/L的碘水,当通入足量Cl2完全反应后,转移的电子为5.0×10-5mol,令碘元素在氧化产物中的化合价为a,则根据电子转移守恒有5.0×10-3L×1.0×10-3mol/L×2×a=5.0×10-5mol,解得a=+5,所以碘单质被氧化为HIO3,则该反应的化学方程式为5Cl2+I2+6H2O=2HIO3+10HCl,
故答案为:5Cl2+I2+6H2O=2HIO3+10HCl;
(3)氨水溶液呈碱性,当加入氨水时,产生BaSO3白色沉淀;当加入HNO3或双氧水时,使溶液中H2SO3氧化成H2SO4,产生BaSO4白色沉淀;而硝酸银溶液与氯化钡溶液生成AgCl白色沉淀,故再加入盐酸、氯化钙溶液始终没有沉淀生成,
故答案为:BD.
(1)实验室常用二氧化锰与浓盐酸反应准备氯气,反应生成氯化锰、氯气与水,反应离子方程式为:MnO2+4H++2Cl-
| ||
故答案为:MnO2+4H++2Cl-
| ||
(2)①二氧化硫与品红化合物无色物质,氯气与水反应生成次氯酸,次氯酸具有强氧化性,将品红氧化为无色物质,二氧化硫与氯气都可以是品红溶液褪色,在装置A中观察到的现象是相同;氯气与铜反应产生棕黄色的烟;二氧化硫在五氧化二钒作催化剂、加热条件下与氧气反应生成三氧化硫,反应方程式为:2SO2+O2
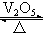 2SO3
2SO3 故答案为:相同;产生棕黄色的烟;2SO2+O2
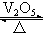 2SO3;
2SO3;②若装置B中装有5.0mL 1.0×10-3mol/L的碘水,当通入足量Cl2完全反应后,转移的电子为5.0×10-5mol,令碘元素在氧化产物中的化合价为a,则根据电子转移守恒有5.0×10-3L×1.0×10-3mol/L×2×a=5.0×10-5mol,解得a=+5,所以碘单质被氧化为HIO3,则该反应的化学方程式为5Cl2+I2+6H2O=2HIO3+10HCl,
故答案为:5Cl2+I2+6H2O=2HIO3+10HCl;
(3)氨水溶液呈碱性,当加入氨水时,产生BaSO3白色沉淀;当加入HNO3或双氧水时,使溶液中H2SO3氧化成H2SO4,产生BaSO4白色沉淀;而硝酸银溶液与氯化钡溶液生成AgCl白色沉淀,故再加入盐酸、氯化钙溶液始终没有沉淀生成,
故答案为:BD.
点评:本题考查元素化合物推断、化学实验、元素化合物性质、常用化学用语、氧化还原反应应用等,(2)中注意根据电子转移守恒计算判断产物,侧重考查学生对知识的综合应用,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目