题目内容
【题目】“星型”聚合物具有独特的结构,在新兴技术领域有广泛的应用。下图是某“星型”聚合物的制备过程。
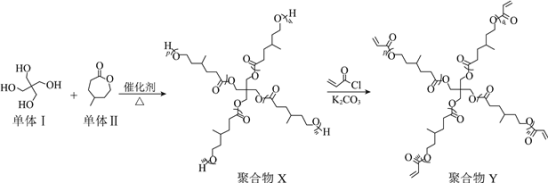
已知:![]()
下列说法不正确的是
A.单体Ⅰ的核磁共振氢谱有两组吸收峰,峰面积比为1∶2
B.单体Ⅰ与单体Ⅱ制备聚合物X,产物中有H2O
C.聚合物X转化为聚合物Y发生取代反应
D.聚合物Y可通过末端的碳碳双键交联形成网状结构
【答案】B
【解析】
A. 有2种等效氢原子,单体Ⅰ的核磁共振氢谱有两组吸收峰,峰面积比为1∶2,故A正确;
有2种等效氢原子,单体Ⅰ的核磁共振氢谱有两组吸收峰,峰面积比为1∶2,故A正确;
B.根据![]() ,单体Ⅰ与单体Ⅱ制备聚合物X,产物中没有H2O,故B错误;
,单体Ⅰ与单体Ⅱ制备聚合物X,产物中没有H2O,故B错误;
C.聚合物X转化为聚合物Y,X中羟基上的H原子被![]() 代替,发生取代反应,故C正确;
代替,发生取代反应,故C正确;
D.聚合物Y的末端都含有碳碳双键,可通过末端的碳碳双键交联形成网状结构,故D正确;
答案选B。

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目