题目内容
(每空1分共计10分)由铜、锌和稀盐酸组成的原电池中,
①铜是 极,发生 反应,电流的方向从 极到 极;锌是 极,发生 反应,电极反应式是 。
②当导线中有1 mol电子通过时,理论上锌片质量 (填增加或减少) g
③铜片上析出
(1)正极 还原 正极到负极 负极 氧化 Zn +2e-=Zn2+
(2)减少 32.5g ③氢气
解析:

练习册系列答案
相关题目
(每空3分共计10分)硫酸工业中废渣称为硫酸渣,其成分为SiO2、Fe2O3、Al2O3、MgO。某探究性学习小组的同学设计以下方案,进行硫酸渣中金属元素的提取实验。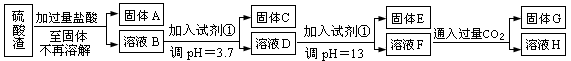
已知溶液pH=3.7时,Fe3+已经沉淀完全;一水合氨电离常数Kb=1.8×10-5,其饱和溶液中c(OH-)约为1×10-3mol·L-1。请回答:
(1)写出A与氢氧化钠溶液反应的化学方程式: 。
(2)上述流程中两次使用试剂①,推测试剂①应该是 (填以下字母编号)
| A.氢氧化钠 | B.氧化铝 | C.氨水 | D.水 |
(4)H中溶质的化学式: ;
(5)计算溶液F中c(Mg2+)= (25℃时,氢氧化镁的Ksp=5.6×10-12)
 上析出
上析出