题目内容
8.相同物质的量的14CO2与S18O2的质量之比为23:34.分析 结合m=nM计算.
解答 解:14CO2与S18O2的摩尔质量分别为46g/mol、68g/mol,设物质的量均为1mol,
则相同物质的量的14CO2与S18O2的质量之比为1mol×46g/mol:1mol×68g/mol=23:34,
故答案为:23:34.
点评 本题考查物质的量的计算,为高频考点,把握物质的量为中心的计算公式为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
18.已知,在2min内某反应物的浓度由3mol/L变成1.5mol/L,则在这段时间内该反应物的化学反应速率为( )
| A. | 3mol/(L•min) | B. | 2mol/(L•min) | C. | 1.5mol/(L•min) | D. | 0.75mol/(L•min) |
19.下列说法正确的是( )
| A. | 煤的干馏和石油的分馏都是物理变化 | |
| B. | 1-氯丙烷和2-氯丙烷的消去产物相同 | |
| C. | 正戊烷、异戊烷、新戊烷的沸点逐渐升高 | |
| D. | 利用油脂在酸性条件下水解,可以生产甘油和肥皂 |
16.X、Y、Z、W为四种短周期元素,它们在周期表中位于连续的四个主族,如图所示.Z元素原子最外层电子数是内层电子总数的$\frac{1}{5}$.下列说法中正确的是( )
| X | Y | ||
| Z | W |
| A. | 原子半径由小到大的顺序为:X<Z<Y<W | |
| B. | Y元素最高价氧化物对应的水化物化学式为H3YO4 | |
| C. | X、Z两种元素的氧化物中所含化学键类型相同 | |
| D. | Y最简单气态氢化物比Y相邻周期同主族元素气态氢化物沸点高 |
3.X、Y、Z、W是短周期中的四种常见元素,其相关信息如表:
(1)Y位于元素周期表第三周期第VIA族,Y和Z的最高价氧化物对应的水化物的酸性较强的是HClO4(写最高价氧化物对应的水化物的化学式).
(2)W可以生成两种氧化物,分别写出这两种氧化物的电子式: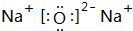 、
、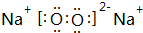 ;
;
(3)用电子式表示Y和 W形成离子化合物的过程 写出X元素的最高价氧化物的电子式
写出X元素的最高价氧化物的电子式 .
.
| 元素 | 相关信息 |
| X | X最外层电子数是次外层电子数的2倍 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的非金属性大于Y |
| W | W的一种核素的质量数为23,中子数为12 |
(2)W可以生成两种氧化物,分别写出这两种氧化物的电子式:
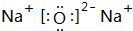 、
、 ;
; (3)用电子式表示Y和 W形成离子化合物的过程
 写出X元素的最高价氧化物的电子式
写出X元素的最高价氧化物的电子式 .
.
20.针对下表中十种元素,填写空格.
(1)最不活泼的元素是Ar.
(2)S原子结构示意图 .
.
(3)N、F、Cl中原子半径最大的是Cl.
(4)最高价氧化物对应水化物酸性最强的是高氯酸(填名称).
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅦA | ⅧA | O |
| 2 | N | O | F | |||||
| 3 | Na | Mg | Al | S | Cl | Ar | ||
| 4 | K | Ca |
(2)S原子结构示意图
 .
.(3)N、F、Cl中原子半径最大的是Cl.
(4)最高价氧化物对应水化物酸性最强的是高氯酸(填名称).
17.下列有关物质的分离与提纯正确的是( )
| A. | 取海带样品,灼烧得灰分,再溶解、过滤得到滤液后加CCl4萃取其中的碘 | |
| B. | 做Fe3+和Cu2+的纸层析实验时,用玻璃棒在标记好的原点处轻轻点样3~5次留下斑点 | |
| C. | 抽滤时,当吸滤瓶内液面高度快达到支管口时,应从支管口倒出溶液 | |
| D. | 除去氯化钠中混有的少量硝酸钾,先将混合物溶于水配成热的饱和溶液,然后蒸发水,当有大量晶体析出时,趁热过滤,硝酸钾留在滤液中 |
18.某化合物为MgmRO3•nH2O(m为正整数),则元素R的化合价为( )
| A. | +(4+m) | B. | +2(m+2) | C. | +(6+m) | D. | +2(3-m) |