题目内容
某化工厂排放的污水中含有Zn2+、Hg2+、Fe3+、Cu2+四种离子。甲、乙、丙三位同学设计从该污水中回收金属铜的方案如下:
甲:![]()
乙: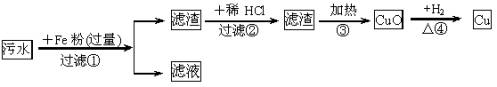
丙: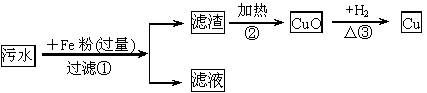
填空和回答:
(1)甲、乙、丙提出的实验方案能制得铜吗?甲 、乙 、丙 (填“能”或“不能”)。
(2)在能制得铜的方案中,哪一步操作会导致环境污染。 。
答案:不能、能、不能;步骤③。
提示:
提示:
甲方案:加入NaOH溶液将Cu2+沉淀的同时,Fe3+、Hg2+也随之沉淀出来,无法得到纯净的Cu(OH)2,而最终不能达到回收铜的目的。 乙方案:加入过量的铁粉,将Cu和Hg置换出来,过滤后滤渣中含有Cu、Hg和过量的铁粉,再加入稀盐酸,铁粉溶解而铜、汞不溶。滤渣中主要是Cu和Hg,加热,Cu生成CuO,Hg变成汞蒸气挥发。用氢气还原氧化铜最终得到纯净的铜。 丙方案:加入过量的铁粉,将铜、汞置换出来。过滤后滤渣中含有铜、汞及过量铁粉,加热铜、铁均形成固体氧化物,无法分开。因此步骤②不能得到纯净的氧化铜,从而最终不能得到纯净的铜。 因为汞蒸气有毒,所以乙方案中步骤③加热汞变成蒸气这一操作会导致环境污染。
|

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目