题目内容
【题目】某无色透明溶液中只可能大量存在NH4+、Na+、Ag+、Ba2+、MnO4-、Fe3+、CO32-、SO42-、NO3-中的几种离子。从其中取两份各100mL,进行如下实验:
(1)不做任何实验就可以肯定原溶液中不存在的两种离子是__、__。
(2)取其中的一份进行实验,加入过量氢氧化钠溶液并加热,生成气体0.06mol。另取其中的一份加入过量Ba(NO3)2溶液,生成白色沉淀4.30g,过滤,向沉淀中再加入过量稀盐酸,沉淀部分消失,余下沉淀2.33g。综上所述说明原溶液中肯定存在的各离子浓度分别是(下面填写要求:例如c(Na+)=0.1mol/L)__、__、__、__。
【答案】MnO4- Fe3+ c(NH4+)=0.6mol/L c(SO42-)=0.1mol/L c(CO32-)=0.1mol/L c(NO3-)≥0.2mol/L
【解析】
(1)MnO4-在溶液中显紫色,Fe3+在溶液中显黄色,题设条件为无色透明溶液,则肯定原溶液中不存在的两种离子是MnO4-、Fe3+,故答案为:MnO4-;Fe3+;
(2)加入过量氢氧化钠溶液并加热,生成的气体为氨气,则n(NH3)=0.06mol,根据关系式可知,原溶液中的铵根离子的物质的量n(NH4+)=n(NH3)=0.06mol,所以c(NH4+)=![]() =0.6mol/L;取其中的一份加入过量Ba(NO3)2,生成白色沉淀4.30g,是碳酸钡和硫酸钡的混合物,一定含有CO32-、SO42-,一定不含Ag+、Ba2+。经过滤,向沉淀中再加入过量稀盐酸,沉淀部分消失,余下沉淀2.33g,因碳酸钡溶于盐酸但是硫酸钡不溶,所以余下沉淀2.33g是硫酸钡,其物质的量是
=0.6mol/L;取其中的一份加入过量Ba(NO3)2,生成白色沉淀4.30g,是碳酸钡和硫酸钡的混合物,一定含有CO32-、SO42-,一定不含Ag+、Ba2+。经过滤,向沉淀中再加入过量稀盐酸,沉淀部分消失,余下沉淀2.33g,因碳酸钡溶于盐酸但是硫酸钡不溶,所以余下沉淀2.33g是硫酸钡,其物质的量是![]() =0.01mol,即原溶液中含有硫酸根离子是0.01mol,c(SO42-)=
=0.01mol,即原溶液中含有硫酸根离子是0.01mol,c(SO42-)=![]() =0.1mol/L;碳酸钡的质量则是4.30g2.33g=1.97g,故碳酸根物质的量为
=0.1mol/L;碳酸钡的质量则是4.30g2.33g=1.97g,故碳酸根物质的量为![]() =0.01mol,所以c(CO32-)=
=0.01mol,所以c(CO32-)=![]() =0.1mol/L;根据电荷守恒可知溶液中必定还存在NO3-,n(NO3-)(0.060.01×2+0.01×2)= 0.02mol,其浓度c(NO3-)
=0.1mol/L;根据电荷守恒可知溶液中必定还存在NO3-,n(NO3-)(0.060.01×2+0.01×2)= 0.02mol,其浓度c(NO3-)![]() =0.2mol/L,故答案为:c(NH4+)=0.6mol/L;c(SO42-)=0.1mol/L;c(CO32-)=0.1mol/L;c(NO3-)≥0.2mol/L。
=0.2mol/L,故答案为:c(NH4+)=0.6mol/L;c(SO42-)=0.1mol/L;c(CO32-)=0.1mol/L;c(NO3-)≥0.2mol/L。

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案【题目】化学一选修:化学与技术磷矿石主要以[Ca3(PO4)2H2O]和磷灰石[Ca5F(PO4)3,Ca5(OH)(PO4)3]等形式存在,图(a)为目前国际上磷矿石利用的大致情况,其中湿法磷酸是指磷矿石用过量硫酸分解制备磷酸,图(b)是热法磷酸生产过程中由磷灰石制单质磷的流程:
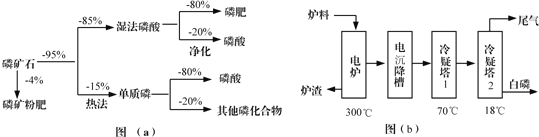
部分物质的相关性质如下:
熔点/℃ | 沸点/℃ | 备注 | |
白磷 | 44 | 280.5 | |
PH3 | -133.8 | -87.8 | 难溶于水、有还原性 |
SiF4 | -90 | -86 | 易水解 |
回答下列问题:
(1)世界上磷矿石最主要的用途是生产含磷肥料,约占磷矿石使用量的____________;
(2)以磷矿石为原料,湿法磷酸过程中Ca5F(PO4)3反应的化学方程式为:___________,现有1t折合含有P2O5约30%的磷灰石,最多可制得到85%的商品磷酸___________t。
(3)如图(b)所示,热法磷酸生产过程的第一步是将SiO2、过量焦炭与磷灰石混合,高温反应生成白磷,炉渣的主要成分是___________(填化学式),冷凝塔1的主要沉积物是___________,冷凝塔2的主要沉积物是___________。
(4)尾气中主要含有___________,还含有少量的PH3、H2S和HF等.将尾气先通入纯碱溶液,可除去___________;再通入次氯酸钠溶液,可除去___________(均填化学式)。
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但优点是___________。