题目内容
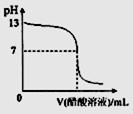 常温下,向10mL 0.1 mol·L-1NaOH溶液中逐滴加入0.1 mol·L-1醋酸溶液,所得滴定曲线如下图所示。下列说法正确的是 ( )
常温下,向10mL 0.1 mol·L-1NaOH溶液中逐滴加入0.1 mol·L-1醋酸溶液,所得滴定曲线如下图所示。下列说法正确的是 ( )
A.pH=7时,所加醋酸溶液的体积为10mL
B.pH<7时,溶液中:c(CH3COO-)>c(Na+)
C.7<pH<13时,溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.继续滴加0.1 mol·L-1醋酸溶液,溶液pH可以变为1
【答案】B
【解析】当NaOH溶液和醋酸恰好完全反应时,生成醋酸钠水解而使溶液显碱性,故A错。当pH<7时有c(H+)>c(OH-),根据电荷守恒可得c(CH3COO-)>c(Na+),故B正确。当7<pH<13时,溶液也有c(Na+)> c(OH-)> c(CH3COO-)>c(H+)这一种情况,C错。对于选项D可作一极端设想,若溶液就是0.1 mol·L-1醋酸,由于醋酸是弱酸,溶液的pH也大于1,故D也错。
【考点】电解质溶液——离子浓度的大小比较

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
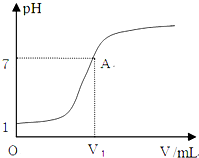 常温下,向10mL 0.1mol?L-1HCl溶液中逐滴加入0.1mol?L-1氨水,所得滴定曲线如图所示.下列说法正确的是( )
常温下,向10mL 0.1mol?L-1HCl溶液中逐滴加入0.1mol?L-1氨水,所得滴定曲线如图所示.下列说法正确的是( )| A、V1=10 mL | B、恰好中和时,溶液中:c(Cl-)≤c(NH4+) | C、A点溶液中存在:c(NH4+)=c(Cl-)=c(OH-)=c(H+) | D、当加入氨水的体积等于或小于10mL时,溶液中可能存在c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
 (2011?南京模拟)常温下,向10mL 0.1mol?L-1NaOH溶液中逐滴加入0.1mol?L-1醋酸溶液,所得滴定曲线如图所示.下列说法正确的是( )
(2011?南京模拟)常温下,向10mL 0.1mol?L-1NaOH溶液中逐滴加入0.1mol?L-1醋酸溶液,所得滴定曲线如图所示.下列说法正确的是( )