题目内容
16.4.48L一定条件下的氯化氢气体通入水中得到0.1L盐酸,此溶液中c(Cl-)=2mol/L,则“一定条件”可能是( )| A. | 25℃ | B. | 1.01×103Pa | C. | 101kPa | D. | 0℃ |
分析 根据溶液中c(Cl-)=2mol/L,n(HCl)=cV=2mol/L×0.1L=0.2mol,
Vm=$\frac{V}{n}$=$\frac{4.48L}{0.2mol}$=22.4L/mol,可知此时为标准状况.
解答 解:根据溶液中c(Cl-)=2mol/L,n(HCl)=cV=2mol/L×0.1L=0.2mol,
Vm=$\frac{V}{n}$=$\frac{4.48L}{0.2mol}$=22.4L/mol,可知此时为标准状况,即为0℃、101kPa;
故选CD.
点评 本题考查气体摩尔体积的适用条件,难度不大,求出气体摩尔体积的数值是判断一定条件的关键.

练习册系列答案
 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
7.(1)CH3+、-CH3(甲基)、CH3-都是重要的有机反应中间体,有关它们的说法正确的是CD.
A.它们均由甲烷去掉一个氢原子所得 B.它们碳原子均采取sp2杂化
C.CH3-与NH3、H3O+几何构型均为三角锥形 D.CH3+中的碳原子采取sp2杂化,所有原子均共面
(2)N2与O22+互为等电子体,O22+的电子式可表示为 ;1mol O22+中含有的π键数目为2NA.
;1mol O22+中含有的π键数目为2NA.
(3)X、Y两种有机物的分子结构和部分物理性质如下表,二者物理性质有差异的主要原因是X物质形成分子内氢键,Y物质形成分子间氢键.
A.它们均由甲烷去掉一个氢原子所得 B.它们碳原子均采取sp2杂化
C.CH3-与NH3、H3O+几何构型均为三角锥形 D.CH3+中的碳原子采取sp2杂化,所有原子均共面
(2)N2与O22+互为等电子体,O22+的电子式可表示为
 ;1mol O22+中含有的π键数目为2NA.
;1mol O22+中含有的π键数目为2NA.(3)X、Y两种有机物的分子结构和部分物理性质如下表,二者物理性质有差异的主要原因是X物质形成分子内氢键,Y物质形成分子间氢键.
| 代号 | 结构简式 | 水中溶解度/g(25℃) | 熔点/℃ | 沸点/℃ |
| X | 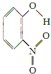 | 0.2 | 45 | 100 |
| Y | 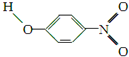 | 1.7 | 114 | 295 |
4.下列有关叙述正确的是( )
| A. | SO2的水溶液能导电,所以SO2是电解质 | |
| B. | BaSO4难溶于水,其水溶液的导电能力极弱,所以BaSO4是弱电解质 | |
| C. | 液溴不导电,所以液溴是非电解质 | |
| D. | HI熔融状态不能导电,但HI是强电解质 |
11.水体中重金属铅的污染问题备受关注.水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、Pb(OH)3-、Pb(OH)42-,各形态的浓度分数α随溶液pH变化的关系如图所示:
[1表示Pb2+、2表示Pb(OH)+、3表示Pb(OH)2、4表示Pb(OH)3-、5表示Pb(OH)42-]
(1)往Pb(NO3)2溶液中滴入稀NaOH溶液,pH=8时溶液存在的阳离子除H+、Na+外,还有:Pb2+、Pb(OH)+.
(2)pH=9时主要反应的离子方程式是:Pb(OH)++OH-?Pb(OH)2↓
(3)某课题组制备了一种新型脱铅剂,能有效去除水中的痕量铅,实验结果如下表:
上表中除 Pb2+外,该脱铅剂对其他离子的去除效果最好的是:Fe3+
(4)如该脱铅剂(用EH表示)脱铅过程中主要发生的反应为:2EH(s)+Pb2+?E2Pb(s)+2H+
则脱铅最合适的pH范围为B(填代码).
A.4~5 B.6~7 C.9~10 D.11~12.
[1表示Pb2+、2表示Pb(OH)+、3表示Pb(OH)2、4表示Pb(OH)3-、5表示Pb(OH)42-]
(1)往Pb(NO3)2溶液中滴入稀NaOH溶液,pH=8时溶液存在的阳离子除H+、Na+外,还有:Pb2+、Pb(OH)+.
(2)pH=9时主要反应的离子方程式是:Pb(OH)++OH-?Pb(OH)2↓
(3)某课题组制备了一种新型脱铅剂,能有效去除水中的痕量铅,实验结果如下表:
| 离子 | Pb2+ | Ca2+ | Fe3+ | Mn2+ | Cl- |
| 处理前浓度(mg/L) | 0.100 | 29.8 | 0.120 | 0.087 | 51.9 |
| 处理后浓度(mg/L) | 0.004 | 22.6 | 0.040 | 0.053 | 49.8 |
(4)如该脱铅剂(用EH表示)脱铅过程中主要发生的反应为:2EH(s)+Pb2+?E2Pb(s)+2H+
则脱铅最合适的pH范围为B(填代码).
A.4~5 B.6~7 C.9~10 D.11~12.

1.NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1molH2中含有的氢原子数为2NA | |
| B. | 22.4L氧气所含的氧原子数为2NA | |
| C. | 常温常压下,28g氮气所含的分子数为2NA | |
| D. | 2g氢气所含的氢原子数为NA |
5.下列变化中必须加入还原剂才能进行的是( )
| A. | H2O→H2 | B. | CuO→Cu | C. | Fe3+→Fe2+ | D. | Zn→Zn2+ |
11.下列电离方程式中,正确的是( )
| A. | NH3•H2O?NH+4+OH- | B. | KClO3=K++Cl-+3O2- | ||
| C. | H2CO3=2H++CO32- | D. | Ba(OH)2=Ba2++OH- |