题目内容
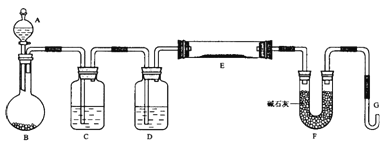
【题目】在炽热条件下,将石蜡油分解产生的乙烯通入下列各试管里,装置如图所示。

根据上述装置,回答下列问题:
(1)C装置的作用是____________。
(2)已知:1,2-二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。预测:A装置中的现象是___________________,B装置中的现象是__________。分离A装置中产物的操作名称是_____,分离B装置中产物需要的玻璃仪器名称是____。
(3)D装置中溶液由紫色变无色,D装置中发生反应的类型为_____。
(4)写出A装置中发生反应的化学方程式_______,反应类型为____,E装置的作用是__________。
【答案】 检验B装置中是否有溴挥发出来 橙色褪去,液体不分层 橙黄色褪去,液体分层 蒸馏 分液漏斗、烧杯、玻璃棒 氧化反应 ![]() 加成反应 检验乙烯与酸性KMnO4溶液反应的产物二氧化碳
加成反应 检验乙烯与酸性KMnO4溶液反应的产物二氧化碳
【解析】
(1)由于溴水易挥发,溴能与硝酸银反应生成溴化银浅黄色沉淀,所以C装置的作用是检验B装置中是否有溴挥发出来。
(2)乙烯与溴发生加成反应生成1,2-二溴乙烷,又因为1,2-二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳,所以A装置中的现象是橙色褪去,液体不分层;乙烯与溴水发生加成反应,则B装置中的现象是橙黄色褪去,液体分层。1,2-二溴乙烷易溶于四氯化碳,二者的沸点相差较大,则分离A装置中产物的操作名称是蒸馏;1,2-二溴乙烷的密度比水的大,难溶于水,则分离B装置中产物是分液操作,需要的玻璃仪器名称是分液漏斗、烧杯、玻璃棒。
(3)D装置中溶液由紫色变无色,说明酸性高锰酸钾溶液被还原,则D装置中发生反应的类型为氧化反应。
(4)根据以上分析可知A装置中发生反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br,反应类型为加成反应。二氧化碳能使澄清石灰水变浑浊,则E装置的作用是检验乙烯与酸性KMnO4溶液反应的产物二氧化碳。

【题目】甲醇是重要的化工原料,又可作为燃料。工业上利用合成气(主要成分为CO、CO2和H2) 在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g) ![]() CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H=-58kJ/mol
CH3OH(g)+H2O(g) △H=-58kJ/mol
③CO2(g)+H2(g) ![]() CO(g)+H2O(g) △H=+41kJ/mol
CO(g)+H2O(g) △H=+41kJ/mol
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
化学键 | H-H | C-O | C=O | H-O | C-H |
E/(kJ/mol) | a | b | c | d | x |
则x=______。(用含表中字母的代数式表示)
(2)若将lmolCO2和2molH2充入容积为2L的恒容密闭容器中,在两种不同温度下发生反应②。测得CH3OH的物质的量随时间的变化如图所示。
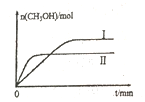
①曲线Ⅰ、Ⅱ对应的平衡常数大小关系为KⅠ_____KⅡ(填“>或“=”或“<”)
②一定温度下,能判断该反应达到化学平衡状态的是______。
a.容器中压强不变
b.甲醇和水蒸气的体积比保持不变
c.v正(H2)=3v逆(CH3OH)
d.2个C=O断裂的同时有3个H-H形成
③若5min后反应达到平衡状态,H2的转化率为90%,则用CO2表示的平均反应速率为_____,该温度下的平衡常数为_____,若容器容积不变,下列措施可增加甲醇产率的是____。
a.升高温度 b.使用合适的催化剂 c.充入He d.按原比例再充入CO2和H2