题目内容
在下列五种物质的组合中,既能跟氢氧化钠溶液反应,又能跟盐酸反应,且在生成物中都有盐和水的是( )
①Al ②Al(OH)3 ③Al2O3 ④Na2CO3 ⑤NaHCO3 ⑥FeO.
①Al ②Al(OH)3 ③Al2O3 ④Na2CO3 ⑤NaHCO3 ⑥FeO.
| A、①②③ | B、①③⑤ |
| C、②③⑤ | D、②④⑤⑥ |
考点:两性氧化物和两性氢氧化物
专题:几种重要的金属及其化合物
分析:既能与氢氧化钠溶液反应又能与盐酸反应,且在生成物中都有盐和水,常见物质有:两性氧化物、两性氢氧化物、弱酸酸式盐、弱酸的铵盐等.
解答:
解:①Al与氢氧化钠溶液反应生成偏铝酸钠与氢气,与盐酸反应生成氯化铝与氢气,没有水生成,故①不符合;
②Al(OH)3与氢氧化钠反应生成偏铝酸钠与水,与盐酸反应生成氯化铝与水,故②符合;
③Al2O3与氢氧化钠反应生成偏铝酸钠与水,与盐酸反应生成氯化铝与水,故③符合;
④Na2CO3不能与氢氧化钠反应,故④不符合;
⑤NaHCO3与氢氧化钠反应生成碳酸钠与水,与盐酸反应生成氯化钠、水与二氧化碳,故⑤符合;
⑥FeO不氢氧化钠溶液反应,故⑥不符合,
故选C.
②Al(OH)3与氢氧化钠反应生成偏铝酸钠与水,与盐酸反应生成氯化铝与水,故②符合;
③Al2O3与氢氧化钠反应生成偏铝酸钠与水,与盐酸反应生成氯化铝与水,故③符合;
④Na2CO3不能与氢氧化钠反应,故④不符合;
⑤NaHCO3与氢氧化钠反应生成碳酸钠与水,与盐酸反应生成氯化钠、水与二氧化碳,故⑤符合;
⑥FeO不氢氧化钠溶液反应,故⑥不符合,
故选C.
点评:本题考查元素化合物性质,难度不大,侧重对基础知识的巩固,注意归纳总结中学常见的既能与酸反应又能与碱反应的物质.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
下列各项表达式正确的是( )
A、S原子的结构示意图: |
| B、过氧化钠的结构式:Na-O-O-Na |
| C、K+离子的核外电子排布式:1s22s22p63s23p6 |
| D、丙烯酸(CH2=CHCOOH)分子中含9个σ键,1个π键 |
一定条件下,通过下列反应可实现燃煤烟气中的硫的回收:SO2(g)+2CO(g)?2CO2(g)+S(l)△H<0
一定温度下,在容积为2L的恒容密闭容器中充入1mol SO2和n mol CO发生反应,5min后达到平衡,生成2a mol CO2.下列说法正确的是( )
一定温度下,在容积为2L的恒容密闭容器中充入1mol SO2和n mol CO发生反应,5min后达到平衡,生成2a mol CO2.下列说法正确的是( )
| A、平衡后保持其它条件不变,从容器中分离出部分硫,平衡向正反应方向移动 |
| B、当混合气体的物质的量不再改变时,反应达到平衡状态 |
| C、平衡后保持其它条件不变,升高温度和加入催化剂,SO2的转化率均增大 |
| D、反应前2min的平均速率v(SO2)=0.1a mol/(L?min) |
能正确表示下列化学反应的离子方程式的是( )
| A、碳酸钙溶于稀盐酸中:CO32-+2H+=H2O+CO2↑ |
| B、澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O |
| C、铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag |
| D、氢氧化钡溶液与盐酸的反应:OH-+H+=H2O |
下列离子方程式中,正确的是( )
| A、石灰石与醋酸反应:CaCO3+2H+=Ca2++CO2↑+H2O |
| B、氧化铁和稀硫酸反应:O2-+2H+=H2O |
| C、向NaHSO4溶液中加入过量的Ba(OH)2溶液:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D、向NaHCO3溶液中加入过量的Ba(OH)2溶液:Ba2++OH-+H++CO32-=BaCO3↓+H2O |
下列物质中,按照只有氧化性、只有还原性,既有氧化性又有还原性的顺序排列的一组是( )
| A、F2、K、HCl |
| B、Cl2、Al、H2 |
| C、NO2、Na、HNO3 |
| D、O2、SO2、H2O |
 HA和HB两种酸的溶液分别加水稀释时,pH变化的简图如图所示,下列叙述中不正确的是( )
HA和HB两种酸的溶液分别加水稀释时,pH变化的简图如图所示,下列叙述中不正确的是( )| A、HA是一种强酸 |
| B、x点,[A-]=[B-] |
| C、HB是一种弱酸 |
| D、原溶液中HA的物质的量浓度为HB的10倍 |
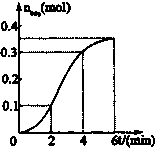 已知CaCO3与稀盐酸的反应为放热反应,取一定量的CaCO3与稀盐酸进行实验,生成CO2的量与反应时间的关系如图所示.下列结论不正确的是( )
已知CaCO3与稀盐酸的反应为放热反应,取一定量的CaCO3与稀盐酸进行实验,生成CO2的量与反应时间的关系如图所示.下列结论不正确的是( )| A、反应开始后2~4分钟内平均反应速率最大 |
| B、反应刚开始时反应速率较小,然后逐渐增大 |
| C、反应前阶段速率逐渐增大,是因为反应放热,使反应速率加快 |
| D、生成物CaCl2、CO2和H2O的总能量比反应物CaCO3和盐酸的总能量高 |
 如图所示为短周期的一部分,如果B原子和C原子的核外电子总数之和为A的4倍,则:
如图所示为短周期的一部分,如果B原子和C原子的核外电子总数之和为A的4倍,则: