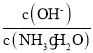题目内容
【题目】钠离子电池具有成本低、能量转换效率高、寿命长等优点。一种钠离子电池用碳基材料(NamCn)作负极,利用钠离子在正负极之间嵌脱过程实现充放电,该钠离子电池的工作原理为:![]()
![]()
![]() 。下列说法不正确的是( )
。下列说法不正确的是( )
A. 充电时,阴极质量减小且Na+数目增加
B. 充电时,阳极的电极反应式为NaCoO2-me-=Na1-mCoO2+mNa+
C. 放电时,Na+向正极移动
D. 放电时,负极的电极反应式为NamCn-me-=mNa++Cn
【答案】A
【解析】
A. 充电时,阴极电极反应式为mNa++Cn+me-=NamCn,阴极电极质量会增大,A项错误;
B. 充电时,阳极上发生失电子的氧化反应,电极反应式为:NaCoO2-me-=Na1-mCoO2+mNa+,B项正确;
C. 放电时阳离子向正极移动,即Na+向正极移动,C项正确;
D. 放电时,负极电极反应式为NamCn-me-=mNa++Cn,D项正确;
答案选A。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】水溶液中的行为是中学化学的重要内容,按要求回答下列问题.
(1)在醋酸水溶液中存在平衡CH3COOH![]() CH3COO-+H+若分别改变下列条件:①加水稀释②加热③加少量固体醋酸钠,其中能使醋酸电离程度增大的是_______,能使溶液pH增大的是_______(填序号)。
CH3COO-+H+若分别改变下列条件:①加水稀释②加热③加少量固体醋酸钠,其中能使醋酸电离程度增大的是_______,能使溶液pH增大的是_______(填序号)。
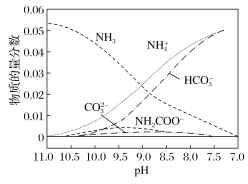
(2)常温下,0.1mol·L-1NaHCO3溶液的pH大于8,则溶液中Na+、HCO3-、CO32-、OH-四种微粒的浓度由大到小的顺序为:________________________________。
(3)AlCl3溶液加热蒸干并灼烧最终得到物质是________(填化学式),将NaHCO3与Al2(SO4)3溶液混合后可做泡沫灭火剂,其原理是_______(用离子方程式表示)。
(4)已知下列物质在20℃下的Ksp如下:
化学式 | AgCl | AgBr | AgI |
颜色 | 白色 | 浅黄色 | 黄色 |
Ksp | 2.0×10-10 | 5.4×10-13 | 8.3×10-17 |
①当向含相同浓度Cl-、Br-、I-的溶液中滴加AgNO3溶液时,_______先沉淀(填离子符号),
②向BaCl2溶液中加入AgNO3和KBr,当两种淀共存时,  =__________。
=__________。