题目内容
下列物质属于含有共价键的离子化合物的是( )
| A.C60 | B.NaOH | C.KF | D.C6H6 |
A、C60是C原子通过共价键形成的单质,故A错误;
B、NaOH属于强碱,是由钠离子和氢氧根离子形成离子化合物,氢氧根离子中,氧原子与氢原子之间形成共价键,故B正确;
C、KF属于盐,由钾离子与氟离子构成,属于离子化合物,但不含共价键,故C错误;
D、C6H6是C原子与H原子通过共价键形成的共价化合物,故D错误;
故选B.
B、NaOH属于强碱,是由钠离子和氢氧根离子形成离子化合物,氢氧根离子中,氧原子与氢原子之间形成共价键,故B正确;
C、KF属于盐,由钾离子与氟离子构成,属于离子化合物,但不含共价键,故C错误;
D、C6H6是C原子与H原子通过共价键形成的共价化合物,故D错误;
故选B.

练习册系列答案
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
下列物质中,属于含有非极性键的共价化合物的是( )
| A、N2 | B、Na2O2 | C、C2H4(乙烯) | D、CH4 |
下列说法正确的是( )
| A、只含有共价键的物质属于共价化合物 | B、所有物质中均含有化学键 | C、含有离子键的物质肯定含金属元素 | D、只要含离子键的化合物就属于离子化合物 |
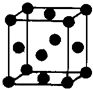 (2012?武汉模拟)[化学一选修 3:物质结构与性质]有U、V、W、X、Y、Z 六种前四周期元素,原子序数依次增大,其相关信息如下表:
(2012?武汉模拟)[化学一选修 3:物质结构与性质]有U、V、W、X、Y、Z 六种前四周期元素,原子序数依次增大,其相关信息如下表: