题目内容
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、22.4 L CO与N2的混合气体中所含原子总数为2NA |
| B、已知2SO2(g)+O2(g)?2SO3(g)△H=-a kJ?mol-1,若将2NA个SO2与NA个O2混合充分反应放出a kJ的热量 |
| C、1 mol CO2分子中共价键总数为2NA |
| D、25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.1NA |
考点:阿伏加德罗常数
专题:
分析:A、气体所处的状态不明确;
B、根据SO2与O2的反应为可逆反应,不能进行彻底来分析;
C、二氧化碳分子中含有两个碳氧双键;
D、25℃时,pH=13的Ba(OH)2溶液中氢氧根离子浓度为0.1mol/L,1L该溶液中含有0.1mol氢氧根离子.
B、根据SO2与O2的反应为可逆反应,不能进行彻底来分析;
C、二氧化碳分子中含有两个碳氧双键;
D、25℃时,pH=13的Ba(OH)2溶液中氢氧根离子浓度为0.1mol/L,1L该溶液中含有0.1mol氢氧根离子.
解答:
解:A、气体所处的状态不明确,故22.4LCO和N2的物质的量不明确,故含有的原子数无法计算,故A错误;
B、SO2与O2的反应为可逆反应,不能进行彻底,故将2NA个SO2与NA个O2混合充分反应后生成的SO3少于2mol,故放出的热量小于a kJ,故B错误;
C、二氧化碳分子中含有两个碳氧双键,1mol CO2分子中共价键总数为4NA.故C错误;
D、25℃时,pH=13的Ba(OH)2溶液中氢氧根离子浓度为0.1mol/L,1.0L溶液中含有0.1mol氢氧根离子,含有的OH-总数为0.1NA,故D正确;
故选D.
B、SO2与O2的反应为可逆反应,不能进行彻底,故将2NA个SO2与NA个O2混合充分反应后生成的SO3少于2mol,故放出的热量小于a kJ,故B错误;
C、二氧化碳分子中含有两个碳氧双键,1mol CO2分子中共价键总数为4NA.故C错误;
D、25℃时,pH=13的Ba(OH)2溶液中氢氧根离子浓度为0.1mol/L,1.0L溶液中含有0.1mol氢氧根离子,含有的OH-总数为0.1NA,故D正确;
故选D.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
下列金属中,遇到强酸或强碱都能放出氢气的是( )
| A、Cu | B、Mg | C、Fe | D、Al |
NA表示阿伏加德常数,下列说法正确的是( )
| A、1mol/L的NaCl溶液中含溶质1mol |
| B、常温常压下,17g氨气所含电子数为10NA |
| C、2.24L氮气所含的原子数为0.2NA |
| D、1molFeCl3形成的氢氧化铁胶体中含有NA个胶粒 |
 某燃煤发电厂的废气中有SO2,它是形成酸雨的罪魁之一.处理SO2一般用生石灰或类似物质来吸收.如图是处理该废气的装置示意图.下列说法不正确的是( )
某燃煤发电厂的废气中有SO2,它是形成酸雨的罪魁之一.处理SO2一般用生石灰或类似物质来吸收.如图是处理该废气的装置示意图.下列说法不正确的是( )| A、此过程中既有分解反应,也有化合反应 |
| B、CaSO4既是氧化产物,又是还原产物 |
| C、使用此废气处理装置可减少酸雨的形成 |
| D、理论上整个过程每转移电子1mol,会对应生成1molCO2 |
下列物质中属于强电解质的是( )
| A、NH3 |
| B、乙醇 |
| C、Cu |
| D、NaCl |
设NA表示阿伏加德罗常数的数值,下列说法中正确的是( )
| A、常温常压下,11.2 L CH4中含有的氢原子数为2 NA |
| B、1 mol Cu被氧化时,失去的电子数一定为2 NA |
| C、1 mol Na2O2与足量水反应后转移的电子数为NA |
| D、0.1 mol/L MgCl2溶液中Cl-离子数为0.2 NA |
下列表示对应化学反应的离子方程式正确的是( )
| A、漂白粉溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O=2HClO+CaSO3↓ |
| B、向苯酚钠溶液中通入少量的CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
| C、Na2O2溶于水产生O2:Na2O2+H2O=2Na++2OH-+O2↑ |
| D、石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O |
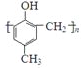 )的合成路线如下:
)的合成路线如下:
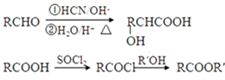 ,F分子式为C7H8O,
,F分子式为C7H8O,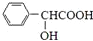 )有多种同分异构体,其中满足下述条件的同分异构体有
)有多种同分异构体,其中满足下述条件的同分异构体有