题目内容
15.酯A水解得甲醇和羧酸B,酯A的相对分子质量为132,又知羧酸B中氧元素质量分数为61.5%,取一定质量的羧酸B完全燃烧生成CO2和H2O的物质的量之比为3:2.则( )| A. | 1mol羧酸B在光照条件下最多可与4mol氯气发生取代反应 | |
| B. | l酯A只能在碱性溶液中才能水解 | |
| C. | 1mol酯A最多可与2mol NaOH溶液发生反应 | |
| D. | 题中酸也能燃烧可知有机物均可在氧气中点燃 |
分析 酯A水解得甲醇和羧酸B,如反应的转化关系为A+H2O→CH3OH+B,酯A的相对分子质量为132,则B的相对分子质量为132+18-32=118,羧酸B中氧元素质量分数为61.5%,则N(O)=$\frac{118×61.5%}{16}$=4.5,不合理,
如为A+2H2O→2CH3OH+B,则B的相对分子质量为132+36-64=104,羧酸B中氧元素质量分数为61.5%,则N(O)=$\frac{104×61.5%}{16}$=4,说明B中含有2个羧基,
取一定质量的羧酸B完全燃烧生成CO2和H2O的物质的量之比为3:2,则n(C):n(H)=3:4,设B的分子式为C3xH4xO4,则有12×3x+4x+64=104,x=1,则
B的分子式为C3H4O4,应为HOOCCH2COOH,A为CH3OOCCH2COOCH3,以此解答该题.
解答 解:酯A水解得甲醇和羧酸B,如反应的转化关系为A+H2O→CH3OH+B,酯A的相对分子质量为134,则B的相对分子质量为132+18-32=118,羧酸B中氧元素质量分数为61.5%,则N(O)=$\frac{118×61.5%}{16}$=4.5,不合理,
如为A+2H2O→2CH3OH+B,则B的相对分子质量为132+36-64=104,羧酸B中氧元素质量分数为61.5%,则N(O)=$\frac{104×61.5%}{16}$=4,说明B中含有2个羧基,
取一定质量的羧酸B完全燃烧生成CO2和H2O的物质的量之比为3:2,则n(C):n(H)=3:4,设B的分子式为C3xH4xO4,则有12×3x+4x+64=104,x=1,则
B的分子式为C3H4O4,应为HOOCCH2COOH,A为CH3OOCCH2COOCH3,
A.B为HOOCCH2COOH,1mol羧酸B在光照条件下最多可与2mol氯气发生取代反应,故A错误;
B.A为酯,可在碱性或酸性条件下水解,故B错误;
C.A为CH3OOCCH2COOCH3,含有2个酯基,则1mol酯A最多可与2mol NaOH溶液发生反应,故C正确;
D.并不是所有的有机物都可燃烧,如CCl4,C的化合价为+4价,不能燃烧,故D错误.
故选C.
点评 本题考查有机物的推断,是高考中的常见题目,题目难度中等,试题基础性强,侧重对学生基础知识的巩固和训练,旨在考查学生灵活运用基础知识解决实际问题的能力,解答本题的关键是把握物质的转化关系.

 名校课堂系列答案
名校课堂系列答案| A. | 碳酸钙和稀盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| B. | 铁粉和稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 向澄清石灰水中通入少量CO2:Ca2++2OH-+CO2═CaCO3↓+H2O | |
| D. | 硫酸铜溶液和氢氧化钡溶液混合:SO42-+Ba2+═BaSO4↓ |
| A. | Ba(OH)2溶液和稀H2SO4的反应 | B. | Cu(OH)2和稀H2SO4的反应 | ||
| C. | NaOH溶液和氢溴酸反应 | D. | NaOH溶液和醋酸溶液的反应 |
 热激活电池可用作火箭、导弹的工作电源.一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法正确的是( )
热激活电池可用作火箭、导弹的工作电源.一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法正确的是( )| A. | 常温时,在正负极间接上电流表或检流计,指针不偏转 | |
| B. | 放电过程中,Li+向负极移动 | |
| C. | 每转移0.2mol电子,理论上生成41.4gPb | |
| D. | 正极反应式:Ca+2Cl--2e-═CaCl2 |
| A. | 单独利用焓变的数据或熵变的数据就能判断化学反应能否自发进行 | |
| B. | 利用一元弱酸的电离平衡常数相对大小可以判断其相应可溶性盐的水解程度的相对大小 | |
| C. | 利用反应热数据的大小可以判断不同反应的反应速率的大小 | |
| D. | 利用溶液的pH与7的大小关系,可以判断任何温度下溶液的酸碱性 |
| A. | 1molCO的质量是28g | B. | HNO3的摩尔质量63g | ||
| C. | ${\;}_{53}^{131}$I 的中子数为53 | D. | H2O和Al3+的核外电子总数不同 |
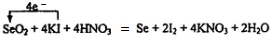 .
. X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素常见单质在常温下都是无色气体,在适当条件下可发生如图所示变化:
X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素常见单质在常温下都是无色气体,在适当条件下可发生如图所示变化: .
.