题目内容
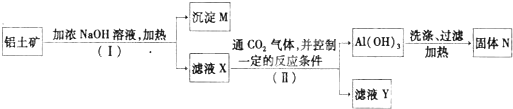
工业上用铝土矿(主要成分是Al2O3·xH2O和少量Fe2O3、SiO2等)提取纯Al2O3作冶炼铝的原料,提取时操作过程如下图所示:
(1)写出滤液A中一种溶质与过量NaOH溶液反应而进入滤液B中的离子方程式:_____
____________________。
(2)在实验①中除去了铝土矿中的__________;在实验②中,除去了铝土矿中的__________;在实验③应加入的是__________,所发生反应的离子方程式为_______________________。
(3)若实验①中不过滤,对后面的操作将产生什么样的影响:________________________。
(4)Al2O3的熔点是2045 ℃,直接受热熔融后通电进行电解冶炼铝,消耗电能太多。工业上采取的措施是熔融冰晶石(Na3AlF6),再加入Al2O3,Al2O3熔融在冰晶石里,然后通电进行电解。试评价这样的措施的意义是什么。
(1)Al3++4OH-====![]() +2H2O
+2H2O
(2)SiO2 Fe2O3 CO2 CO2+2H2O+![]() ====Al(OH)3↓+
====Al(OH)3↓+![]()
(3)将不能除去SiO2 (4)降低对设备的要求,节约能源

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目