题目内容
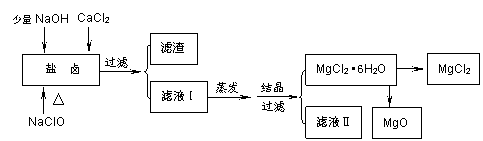
(16分)广东省有着丰富的海洋资源。海水提取食盐和Br2以后的盐卤可以用来制备纯净的MgCl2或MgO。盐卤中含有Mg2+、Cl-,还含有少量Na+、Fe2+、Fe3+、SO42- 等。制备流程如下图
(1)滤液Ⅱ中所含主要的杂质离子是 (写离子符号)。
(2) 加入NaClO的作用是 。
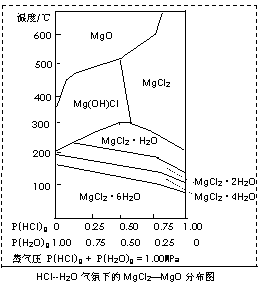
(3)温度和压强P(HCl)g对MgCl2·6H2O晶体热分解产物的影响如图所示。
请回答下列问题:
①写出P(HCl)g = 0.25MPa,温度从300℃升高到550℃时反应的化学方程式 ;
②实际生产中,将MgCl2·6H2O晶体加热到600℃的过程中几乎得不到无水MgCl2,其原因是
;若要得到无水MgCl2须采取的措施是 。
(1)Na+
(2)将Fe2+ 氧化为 Fe3+ ,并形成Fe(OH)3 被除去
(3)① Mg(OH)Cl MgO + HCl↑
②P(HCl)小,加热时 Mg2+ 会发生水解
通入HCl,增大P(HCl,抑制 Mg2+水解
解析:略

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目