题目内容
已知室温时,0.1 mol/L某一元酸HA在水中有0.1%发生电离,回答下列问题:
(1)该溶液中c(H+)= 。
(2)HA的电离平衡常数K= ;
(3)升高温度时,K (填“增大”,“减小”或“不变”)。
(4)由HA电离出的c(H+)约为水电离出的c(H+)的 倍。
(1)该溶液中c(H+)= 。
(2)HA的电离平衡常数K= ;
(3)升高温度时,K (填“增大”,“减小”或“不变”)。
(4)由HA电离出的c(H+)约为水电离出的c(H+)的 倍。
(1)1.0×10-4 mol/L
(2)1×10-7
(3)增大 (4)106
(2)1×10-7
(3)增大 (4)106
(1)HA电离出的c(H+)=0.1×0.1% mol/L=1×10-4 mol/L;
(2)电离平衡常数
K=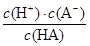 =
=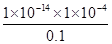 =1×10-7;
=1×10-7;
(3)因HA的电离是吸热过程,升高温度c(H+)、c(A-)均增大,则K增大;
(4)c(H+)HA=1×10-4 mol/L,c(H+)水=c(OH-)=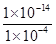 =1×10-10 mol/L,所以c(H+)HA∶c(H+)水=(1×10-4)∶(1×10-10)=106。
=1×10-10 mol/L,所以c(H+)HA∶c(H+)水=(1×10-4)∶(1×10-10)=106。
(2)电离平衡常数
K=
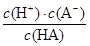 =
=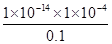 =1×10-7;
=1×10-7;(3)因HA的电离是吸热过程,升高温度c(H+)、c(A-)均增大,则K增大;
(4)c(H+)HA=1×10-4 mol/L,c(H+)水=c(OH-)=
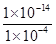 =1×10-10 mol/L,所以c(H+)HA∶c(H+)水=(1×10-4)∶(1×10-10)=106。
=1×10-10 mol/L,所以c(H+)HA∶c(H+)水=(1×10-4)∶(1×10-10)=106。
练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
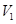 LpH=11的NaOH溶液与
LpH=11的NaOH溶液与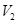 LpH=3的HA溶液混合后显中性,则
LpH=3的HA溶液混合后显中性,则 )>c(SO
)>c(SO )>c(H2SO3)。则该溶液中c(H+) c(OH-) (填“大于”、“小于”或“等于”),简述理由: .
)>c(H2SO3)。则该溶液中c(H+) c(OH-) (填“大于”、“小于”或“等于”),简述理由: . H++HCO3—,则溶液的pH约为( )
H++HCO3—,则溶液的pH约为( )