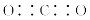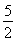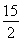��Ŀ����
T Kʱ����2.0 L�����ܱ������г���1.0 mol COCl2����ӦCOCl2��g�� Cl2��g����CO��g��������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
Cl2��g����CO��g��������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
t/s | 0 | 2 | 4 | 6 | 8 |
n��Cl2��/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
����˵����ȷ���ǣ���������
A����Ӧ��ǰ2 s ��ƽ������v��CO����0.080 mol��L��1��s��1
B�����������������䣬�����¶ȣ�ƽ��ʱ��c��Cl2����0.11 mol��L��1����Ӧ����H��0
C��T Kʱ��ʼ�������г���0.9 mol COCl2��0.10 mol Cl2 ��0.10 mol CO����Ӧ�ﵽƽ��ǰv����v��
D��T Kʱ��ʼ�������г���1.0 mol Cl2��0.9 mol CO���ﵽƽ��ʱ��Cl2��ת����С��80%
CD
��������v��CO����v��Cl2���� ��0.040 mol��L��1��s��1��A����ע�����������Ϊ2 L��ԭƽ��״̬ʱ��c��Cl2����0.1 mol��L��1���¶����ߺ�c��Cl2������ƽ�������ƶ����ó�����ӦΪ���ȷ�Ӧ��B����ԭƽ��״̬ʱ��K��
��0.040 mol��L��1��s��1��A����ע�����������Ϊ2 L��ԭƽ��״̬ʱ��c��Cl2����0.1 mol��L��1���¶����ߺ�c��Cl2������ƽ�������ƶ����ó�����ӦΪ���ȷ�Ӧ��B����ԭƽ��״̬ʱ��K��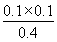 ��0.025�������¶Ȳ��䣬��K���䣬Q��
��0.025�������¶Ȳ��䣬��K���䣬Q�� ��0.005 6��K������ƽ��Ӧ������Ӧ�����ƶ�����v����v����C��ȷ��ԭƽ��ʱCOCl2��ת���ʣ�
��0.005 6��K������ƽ��Ӧ������Ӧ�����ƶ�����v����v����C��ȷ��ԭƽ��ʱCOCl2��ת���ʣ�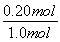 ��100%��20%������ʼ����1.0 mol Cl2��1.0 mol CO���ﵽƽ��ʱCl2ת����Ϊ80%�����ٳ���0.1 mol CO����Cl2ת���ʼ�С��D��ȷ��
��100%��20%������ʼ����1.0 mol Cl2��1.0 mol CO���ﵽƽ��ʱCl2ת����Ϊ80%�����ٳ���0.1 mol CO����Cl2ת���ʼ�С��D��ȷ��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�