��Ŀ����
��6�֣���1����һ��������N2��H2��Ӧ����NH3����ش�
������Ӧ���������ΪE1���������������ΪE2����E1 >E2����÷�ӦΪ ������ȡ����ȡ�����Ӧ��
����֪��1mol H��H����1molN��H����1molN��N���ֱ���Ҫ��������436kJ��391kJ��946kJ����N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ________________________________��
��2�����ݸ�˹���ɿ��Զ�ijЩ����ͨ��ʵ��ֱ�Ӳⶨ�Ļ�ѧ��Ӧ���ʱ�������㡣
��֪��C(s��ʯī)��O2(g)��CO2(g) ��H1��Q1kJ��mol��1
2CO2(g)��H2 (g)��C2H2(g)��2O2(g) ��H2��Q2kJ��mol��1�����ݸ�˹���ɣ������ʱ��C(s��ʯī)��H2(g)����1mol C2H2(g)��Ӧ���ʱ�Ϊ kJ��mol��1���ú���Q1��Q2��ʽ�ӱ�ʾ����
��1���� ���� ��1�֣� �� N2(g)+ 3H2(g)  2NH3(g) ��H=��92 kJ��mol-1 ��3�֣�
2NH3(g) ��H=��92 kJ��mol-1 ��3�֣�
��2�� 2Q1+Q2 ��2�֣�
����

��ϰ��ϵ�д�
�����Ŀ
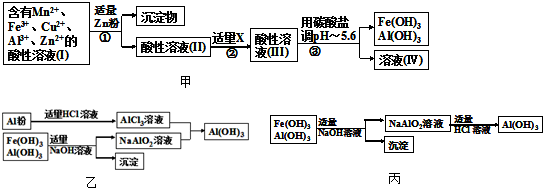



 ��
�� ��
�� ��
��
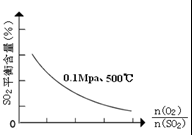 ��1����һ�������£���һ�ݻ��ɱ���ܱ������У���SO2��O2��Ϸ�����Ӧ��
��1����һ�������£���һ�ݻ��ɱ���ܱ������У���SO2��O2��Ϸ�����Ӧ��