题目内容
【题目】某强酸性溶液X中可能含有Fe2+、Fe3+、A13+、Ba2+、NH4+、CO32-、NO3ˉ、SO42-、SiO32-中的若干种,现取X溶液进行连续实验,实验过程及产物如图所示。实验过程中有一种气体为红棕色。
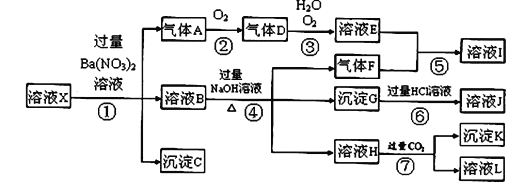
根据以上信息,回答下列问题:
(1)由强酸性条件即可判断X溶液中肯定不存在的离子有____________________。
(2)溶液X中关于硝酸根离子的判断,正确的是_______;(填编号,下同)
a. 一定含有 b. 一定不含有 c.可能含有
(3)气体F的电子式为__________,化合物I中含有的化学键类型有________;
(4)转化⑦的离子方程式为_________________________________________;
(5)对不能确定是否存在的离子,可以另取X溶液,加入下列溶液中的一种,根据现象即可判断,该试剂最好是_________。
①NaOH溶液 ②KSCN溶液 ③氯水和KSCN的混合溶液 ④pH试纸 ⑤KMnO4溶液
【答案】 CO32-、SiO32- b 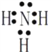 共价键和离子键 [Al(OH)4]ˉ+ CO2= HCO3ˉ+ Al(OH)3↓或AlO2ˉ+2H2O+ CO2= HCO3ˉ+ Al(OH)3↓ ②
共价键和离子键 [Al(OH)4]ˉ+ CO2= HCO3ˉ+ Al(OH)3↓或AlO2ˉ+2H2O+ CO2= HCO3ˉ+ Al(OH)3↓ ②
【解析】(1)在强酸性溶液中氢离子和碳酸根离子反应生成二氧化碳和水,硅酸根离子和氢离子反应生成硅酸沉淀,所以一定不会存在CO32-、SiO32-离子;
(2)加入过量硝酸钡生成沉淀,钡离子和硫酸根离子反应生成硫酸钡沉淀,说明一定含有SO42-,含有SO42-离子就一定不含Ba2+离子;气体A连续氧化生成D和E,则A为NO,D为NO2,E为HNO3,说明溶液中含有还原性离子,一定为Fe2+,则在酸性条件下一定不含NO3ˉ离子,否则酸性条件下NO3ˉ会将Fe2+氧化而不能大量共存,答案选b;(3)溶液B中加入过量NaOH溶液 并加热,生成气体F,则F为NH3,其电子式为:![]() ;溶液E为HNO3,气体F为NH3,E与F反应生成I为NH4NO3,含有的化学键类型有离子键和极性共价键;(4)根据题中提供的离子,前面已排除SiO32-的存在,则在过量氢氧化钠作用下得到的溶液H,通入过量二氧化碳后能产生沉淀K,K应该为氢氧化铝,则溶液H中含有偏铝酸根离子,故溶液X中含有A13+,转化⑦的离子方程式为[Al(OH)4]ˉ + CO2 = HCO3ˉ + Al(OH)3↓或AlO2ˉ+2H2O+ CO2 = HCO3ˉ + Al(OH)3↓;(5)综上可知,溶液中一定含有Fe2+、A13+、NH4+、NO3ˉ、SO42-,一定不含有Ba2+、CO32-、SiO32-,不能确定是否含有Fe3+,最好选择KSCN溶液对Fe3+离子进行检验,答案选②。
;溶液E为HNO3,气体F为NH3,E与F反应生成I为NH4NO3,含有的化学键类型有离子键和极性共价键;(4)根据题中提供的离子,前面已排除SiO32-的存在,则在过量氢氧化钠作用下得到的溶液H,通入过量二氧化碳后能产生沉淀K,K应该为氢氧化铝,则溶液H中含有偏铝酸根离子,故溶液X中含有A13+,转化⑦的离子方程式为[Al(OH)4]ˉ + CO2 = HCO3ˉ + Al(OH)3↓或AlO2ˉ+2H2O+ CO2 = HCO3ˉ + Al(OH)3↓;(5)综上可知,溶液中一定含有Fe2+、A13+、NH4+、NO3ˉ、SO42-,一定不含有Ba2+、CO32-、SiO32-,不能确定是否含有Fe3+,最好选择KSCN溶液对Fe3+离子进行检验,答案选②。

 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案