题目内容
一定条件下,在一固定容积密闭容器中发生如下反应:N2(g)+3H2(g)?2NH3(g),若开始时只充入2a mol NH3,达到平衡时,混合气体的压强比起始时增大了40%.若开始时充入a mo N2和3a mol H2的混合气体,求:
(1)达到平衡时H2的转化率
(2)平衡时NH3在混合气体中的体积分数
(1)达到平衡时H2的转化率
60%
60%
;(2)平衡时NH3在混合气体中的体积分数
42.9%
42.9%
.分析:N2 (g)+3H2(g) 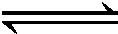 2NH3 (g)
2NH3 (g)
起始(mol) 0 0 2a
反应(mol) x 3x 2x
平衡(mol) x 3x (2a-2x)
达到平衡时,混合气体的压强比起始时增大了40%,
则
=1.4,解得x=0.4a,
以此计算转化率和气体的体积分数.
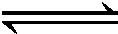 2NH3 (g)
2NH3 (g)起始(mol) 0 0 2a
反应(mol) x 3x 2x
平衡(mol) x 3x (2a-2x)
达到平衡时,混合气体的压强比起始时增大了40%,
则
| x+3x+(2a-2x) |
| 2a |
以此计算转化率和气体的体积分数.
解答:解:N2 (g)+3H2(g) 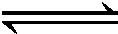 2NH3 (g)
2NH3 (g)
起始(mol) 0 0 2a
反应(mol) x 3x 2x
平衡(mol) x 3x (2a-2x)
达到平衡时,混合气体的压强比起始时增大了40%,
则
=1.4,解得x=0.4a,
(1)若开始时充入a mol N2和3a mol H2的混合气体,达到平衡时,与开始充入2a mol NH3平衡等效,
所以反应的H2的物质的量为:3a-3x=3a-3×0.4a=1.8amol,则H2的转化率为
×100%=60%,
故答案为:60%;
(2)NH3在混合气体中的体积分数为
×100%=42.9%,故答案为:42.9%.
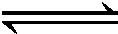 2NH3 (g)
2NH3 (g)起始(mol) 0 0 2a
反应(mol) x 3x 2x
平衡(mol) x 3x (2a-2x)
达到平衡时,混合气体的压强比起始时增大了40%,
则
| x+3x+(2a-2x) |
| 2a |
(1)若开始时充入a mol N2和3a mol H2的混合气体,达到平衡时,与开始充入2a mol NH3平衡等效,
所以反应的H2的物质的量为:3a-3x=3a-3×0.4a=1.8amol,则H2的转化率为
| 1.8a |
| 3a |
故答案为:60%;
(2)NH3在混合气体中的体积分数为
| 2a-2×0.4a |
| 0.4a+1.2a+1.2a |
点评:本题考查化学平衡的计算,明确化学平衡三段法计算方法及等效平衡是解答本题的关键,注意两平衡中平衡时量相同,题目难度中等.

练习册系列答案
相关题目
 CH3OCH3(g)+3H2O(g);△H<0.
CH3OCH3(g)+3H2O(g);△H<0.
 2NH3(g),若开始时只充入2a mol NH3,达到平衡时,混合气体的压强比起始时增大了40%。若同条件下开始时充入a mo N2和3a mol H2的混合气体,求:
2NH3(g),若开始时只充入2a mol NH3,达到平衡时,混合气体的压强比起始时增大了40%。若同条件下开始时充入a mo N2和3a mol H2的混合气体,求: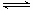 2NH3(g),若开始时只充入2a mol NH3,达到平衡时,混合气体的压强比起始时增大了40%。若开始时充入a mo N2和3a mol H2的混合气体,求:
2NH3(g),若开始时只充入2a mol NH3,达到平衡时,混合气体的压强比起始时增大了40%。若开始时充入a mo N2和3a mol H2的混合气体,求: 2NH3(g),若开始时只充入2a mol NH3,达到平衡时,混合气体的压强比起始时增大了40%。若开始时充入a mo N2和3a mol H2的混合气体,求:
2NH3(g),若开始时只充入2a mol NH3,达到平衡时,混合气体的压强比起始时增大了40%。若开始时充入a mo N2和3a mol H2的混合气体,求: