题目内容
1.在常温下,将一定量的铜均分为两等份.一份完全溶于一定量浓硝酸,产生NO2、N2O4、NO的混合气体,这些气体若与2.24L O2(标准状况)混合后通入水中,气体被水完全吸收.将另一份铜加入到500mL18mol•L-1的浓H2SO4溶液中,则可溶解的Cu的质量为( )| A. | 0 g | B. | 32 g | C. | 38.4 g | D. | 48 g |
分析 常温下铜与浓硫酸不反应,由此分析解答.
解答 解:常温下铜与浓硫酸不反应,所以铜加入到500mL18mol•L-1的浓H2SO4溶液中,不反应,消耗Cu的质量为0g,
故选A.
点评 本题考查铜与浓硫酸,硝酸反应的有关判断与计算,学生要清楚铜与浓硫酸反应要在加热的条件下进行,通过定性判断解题,比较容易.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
11.设NA代表阿伏伽德罗常数的数值,则下列说法正确的是( )
| A. | 1mol十八烷分子中含有的共价键的数目为54NA | |
| B. | 21g乙烯和丙烯的混合物中所含原子个数为4.5NA | |
| C. | 标准状况下,22.4L的一氯甲烷和二氯甲烷的混合物所含原子的数目为4NA | |
| D. | 1mol/LNa2CO3溶液中,Na+的数目为2NA |
6.氯的原子序数为17,37Cl和35Cl是氯的两种同位素,下列说法正确的是( )
| A. | 35Cl原子所含质子数为18,37Cl和35Cl得电子能力相同 | |
| B. | $\frac{1}{18}$mol的H35Cl分子所含中子数约为6.02×1023 | |
| C. | 7 g的35Cl2气体的体积为2.24 L | |
| D. | 35Cl的相对原子质量是12C原子质量的35倍 |
13.糖类、油脂和蛋白质是维持人体生命活动所必需的三大营养物质,以下叙述正确的是( )
| A. | 蛋白质中至少含有四种元素 | |
| B. | 用饱和的CuSO4溶液使蛋清液发生盐析,进而分离、提纯蛋白质 | |
| C. | 所有的糖类、油脂和蛋白质均能发生水解反应 | |
| D. | 油脂在稀硫酸催化条件下的水解又叫皂化反应 |
10.硅元素在周期表中的位置是( )
| A. | 第二周期IVA族 | B. | 第三周期IVA族 | C. | 第三周期VIA族 | D. | 第二周期VIA族 |
11.在恒温恒容条件下,2NO+O2?2NO2达到平衡的标志是( )
| A. | NO、O2、NO2分子数目比是2:1:2 | |
| B. | 反应混合物中各组分物质的浓度相等 | |
| C. | 混合气体的总质量不变 | |
| D. | 混合气体的平均相对分子质量不变 |
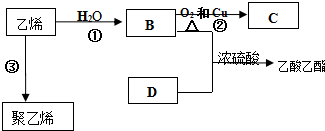

 .
.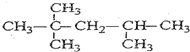 .
.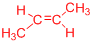 .
.