题目内容
下列实验中所选用的仪器合理的是________
- A.用200 mL量筒量取5.2 mL稀硫酸
- B.用100 mL烧杯配制100 g质量分数为1%的食盐水
- C.用托盘天平称量11.7 g氯化钠晶体
- D.用碱式滴定管量取25.1 mL溴水
- E.用瓷坩埚灼烧Na、Na2O、NaOH等
- F.用250 mL容量瓶配制250 mL 0.2 mol·L-1的氢氧化钠溶液
1.
2. CF
试题分析:选用量筒时,应选择与所要量取的液体体积最接近的量筒为最好,A不正确;B中烧杯的容积太小;D中有两处错误:一是不能用碱式滴定管来量取溴水,因为溴水氧化性较强,可腐蚀橡胶管,二是滴定管的准确度是0.01 mL而不是0.1 mL,故应是25.10 mL;在高温下Na2O、NaOH等物质可以与瓷坩埚中的成分SiO2反应而腐蚀坩埚,故E也不正确,即答案选CF。
点评:化学实验常用仪器的使用方法和化学实验基本操作是进行化学实验的基础,对化学实验的考查离不开化学实验的基本操作,所以该类试题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。
2. CF
试题分析:选用量筒时,应选择与所要量取的液体体积最接近的量筒为最好,A不正确;B中烧杯的容积太小;D中有两处错误:一是不能用碱式滴定管来量取溴水,因为溴水氧化性较强,可腐蚀橡胶管,二是滴定管的准确度是0.01 mL而不是0.1 mL,故应是25.10 mL;在高温下Na2O、NaOH等物质可以与瓷坩埚中的成分SiO2反应而腐蚀坩埚,故E也不正确,即答案选CF。
点评:化学实验常用仪器的使用方法和化学实验基本操作是进行化学实验的基础,对化学实验的考查离不开化学实验的基本操作,所以该类试题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。

练习册系列答案
相关题目
Ⅰ.下图为常见仪器的部分结构(有的仪器被放大)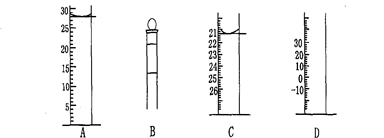
图A中液面所示溶液的体积为 mL,用上述四种仪器中的某种测量一液体的体积,平视时读数为n mL,仰视时读数为m mL,若m>n,则所使用的仪器是 (填字母标号)。
Ⅱ.某学生用标准0.25 mol·L—1 NaOH溶液滴定硫酸的实验操作如下:
| A.用酸式滴定管取稀H2SO4 25.00 mL,注入锥形瓶中,加入指示剂。 | |
| B.用待测定的溶液润洗酸式滴定管。 | C.用蒸馏水洗干净滴定管。 |
| D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3 cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下。 |
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。
①滴定操作的正确顺序是(用序号填): 。
②该滴定操作中应选用的指示剂是: 。
③在G操作中如何确定终? 。
④碱式滴定管用蒸馏水润洗后,未用标准液润洗导致滴定结果(填“偏小”、“偏大”或“恰好合适”) ,原因是 。
⑤假设操作均正确,标准液消耗了22.18mL,计算待测硫酸溶液的物质的量浓度(计算结果精确到小数点后二位) mol·L—1
Ⅲ.已知常温时醋酸的电离常数为1.8×10-5,一水合氨的电离常数为1.8×10-5。在少量Mg(OH)2悬浊液中,滴加适量饱和NH4Cl溶液,固体溶解。对于固体的溶解。
甲同学认为在氢氧化镁悬浊液中存在下列平衡:
Mg(OH)2
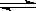 Mg2+ +2OH-
Mg2+ +2OH-加入NH4Cl溶液,由于NH4+水解产生H+中和了Mg(OH)2电离产生的OH-而使平衡右移导致Mg(OH)2 溶解。
而乙同学却认为NH4Cl电离产生的NH4+结合了OH-生成了弱电解质NH3·H2O,使c(OH-)减小,平衡右移而导致Mg(OH)2 溶解。设计方案评价甲乙两位同学的观点:
_____________________________________ ______________________________
_________________________________________________________________________
 仪器如图所示(装置可重复使用)。回答下列问题:
仪器如图所示(装置可重复使用)。回答下列问题:

 Mg2+ +2OH-
Mg2+ +2OH-