题目内容
0.1mol?L-1BaCl2溶液100mL,和0.08mol?L-1AgNO3溶液1000mL充分混合后又加入0.06mol?L-1 ZnSO41000mL,最后溶液中浓度最大的离子是
- A.Cl-
- B.Zn2+
- C.Ag+
- D.NO3-
D
分析:最后溶液的体积相同,比较溶液中离子的物质的量进行离子浓度大小比较.
0.1mol?L-1BaCl2溶液100mL中n(Ba2+)=0.01mol,n(Cl-)=0.02mol;
0.08mol?L-1AgNO3溶液1000mL中n(Ag+)=0.08mol,n(NO3-)=0.08mol,
0.06mol?L-1 ZnSO41000mL中n(Zn2+)=0.06mol,n(SO42-)=0.06mol,
BaCl2溶液和AgNO3溶液混合,首先发生反应:Ag++Cl-=AgCl↓,氯离子有剩余,上述混合溶液再加入ZnSO4溶液,发生反应Ba2++SO42-=BaSO4↓,据此计算反应后溶液的离子物质的量进行判断.
解答:0.1mol?L-1BaCl2溶液100mL中n(Ba2+)=0.01mol,n(Cl-)=0.02mol
0.08mol?L-1AgNO3溶液1000mL中n(Ag+)=0.08mol,n(NO3-)=0.08mol,
BaCl2溶液和AgNO3溶液混合,首先发生反应:Ag++Cl-=AgCl↓,氯离子有剩余,反应后溶液中n(Cl-)=0.02mol-0.08mol=0.12mol,n(Ba2+)=0.01mol,n(NO3-)=0.08mol,
上述混合溶液再加入ZnSO4溶液,0.06mol?L-1 ZnSO41000mL中n(Zn2+)=0.06mol,n(SO42-)=0.06mol,发生反应Ba2++SO42-=BaSO4↓,硫酸根有剩余,
故反应后溶液中n(SO42-)=0.06mol-0.01=0.05,n(Zn2+)=0.06mol,n(Cl-)=0.12mol,n(NO3-)=0.08mol,
故溶液中NO3-浓度最大,故选D.
点评:本题考查物质的量浓度计算、离子反应的有关计算等,难度中等,可以比较起始离子的物质的量,结合硝酸根不反应直接得出答案,更为简单.
分析:最后溶液的体积相同,比较溶液中离子的物质的量进行离子浓度大小比较.
0.1mol?L-1BaCl2溶液100mL中n(Ba2+)=0.01mol,n(Cl-)=0.02mol;
0.08mol?L-1AgNO3溶液1000mL中n(Ag+)=0.08mol,n(NO3-)=0.08mol,
0.06mol?L-1 ZnSO41000mL中n(Zn2+)=0.06mol,n(SO42-)=0.06mol,
BaCl2溶液和AgNO3溶液混合,首先发生反应:Ag++Cl-=AgCl↓,氯离子有剩余,上述混合溶液再加入ZnSO4溶液,发生反应Ba2++SO42-=BaSO4↓,据此计算反应后溶液的离子物质的量进行判断.
解答:0.1mol?L-1BaCl2溶液100mL中n(Ba2+)=0.01mol,n(Cl-)=0.02mol
0.08mol?L-1AgNO3溶液1000mL中n(Ag+)=0.08mol,n(NO3-)=0.08mol,
BaCl2溶液和AgNO3溶液混合,首先发生反应:Ag++Cl-=AgCl↓,氯离子有剩余,反应后溶液中n(Cl-)=0.02mol-0.08mol=0.12mol,n(Ba2+)=0.01mol,n(NO3-)=0.08mol,
上述混合溶液再加入ZnSO4溶液,0.06mol?L-1 ZnSO41000mL中n(Zn2+)=0.06mol,n(SO42-)=0.06mol,发生反应Ba2++SO42-=BaSO4↓,硫酸根有剩余,
故反应后溶液中n(SO42-)=0.06mol-0.01=0.05,n(Zn2+)=0.06mol,n(Cl-)=0.12mol,n(NO3-)=0.08mol,
故溶液中NO3-浓度最大,故选D.
点评:本题考查物质的量浓度计算、离子反应的有关计算等,难度中等,可以比较起始离子的物质的量,结合硝酸根不反应直接得出答案,更为简单.

练习册系列答案
相关题目
Na2SO3是抗氧剂.向烧碱和Na2SO3的混合溶液中加入少许溴水,振荡后溶液变为无色.
(1)SO2通入过量NaOH溶液可得到烧碱和Na2SO3的混合溶液,该反应的化学方程式为 .
(2)碱性条件下Br2与Na2SO3溶液反应的离子方程式为 ,该反应的氧化剂是 ,1mol Br2参与反应转移 mol电子.
(3)反应后的溶液含有SO32-、SO42-、Br-、OH-等阴离子,请填写鉴定其中SO32-、SO42-和Br-的实验报告.
限选试剂:2mol?L-1HCl;1mol?L-1H2SO4;1mol?L-1BaCl2;1mol?L-1Ba(NO3)2;0.1mol?L-1AgNO3;CCl4;新制饱和溴水;新制饱和氯水.
(1)SO2通入过量NaOH溶液可得到烧碱和Na2SO3的混合溶液,该反应的化学方程式为
(2)碱性条件下Br2与Na2SO3溶液反应的离子方程式为
(3)反应后的溶液含有SO32-、SO42-、Br-、OH-等阴离子,请填写鉴定其中SO32-、SO42-和Br-的实验报告.
限选试剂:2mol?L-1HCl;1mol?L-1H2SO4;1mol?L-1BaCl2;1mol?L-1Ba(NO3)2;0.1mol?L-1AgNO3;CCl4;新制饱和溴水;新制饱和氯水.
| 编号 | 实验操作 | 预期现象和结论 | ||
| 步骤① | 取少量待测液于试管A中,D滴加2mol?L-1HCl至溶液呈酸性,加入几滴 |
证明待测液中含SO
| ||
| 步骤② | 有白色沉淀生成证明待测液中含SO
| |||
| 步骤③ | 另取少量待测液于试管C中,加入足量氯水,再加入四氯化碳,震荡,静置后观察颜色 | 待测液中含Br- |
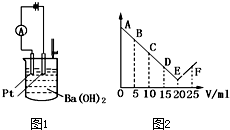 如图1所示:将30ml 0.1mol?L-1Ba(OH)2溶液置于烧杯中,然后慢慢加入0.1mol?L-1某第三周期元素形成的某酸溶液共25mL,加入酸溶液的体积V与电流强度I的I-V图如图2所示.
如图1所示:将30ml 0.1mol?L-1Ba(OH)2溶液置于烧杯中,然后慢慢加入0.1mol?L-1某第三周期元素形成的某酸溶液共25mL,加入酸溶液的体积V与电流强度I的I-V图如图2所示.