题目内容
20.某对酸性溶液进行下列操作:①灼烧,火焰呈蓝色;②加BaCl2出现白色沉淀;③浓缩后加浓H2SO4和铜片共热产生红棕色气体,则此溶液中,可能存在的离子是( )| A. | Na+、SO${\;}_{4}^{2-}$、NO${\;}_{3}^{-}$ | B. | K+、NO${\;}_{3}^{-}$、CO${\;}_{3}^{2-}$ | ||
| C. | Na+、K+、SO${\;}_{3}^{2-}$ | D. | Na+、NO${\;}_{3}^{-}$、SO${\;}_{3}^{2-}$ |
分析 酸性溶液一定含有氢离子,①灼烧,火焰呈蓝色;②加BaCl2出现白色沉淀,说明含有硫酸根离子或银离子;③浓缩后加浓H2SO4和铜片共热产生红棕色气体,说明含有硝酸根离子,据此分析解答.
解答 解:酸性溶液一定含有氢离子,这说明一定不含有CO32-,一定不含有SO32-,①灼烧,火焰呈蓝色不能确定离子;②加BaCl2出现白色沉淀;说明含有硫酸根离子或银离子,③浓缩后加浓H2SO4和铜片共热产生红棕色气体NO2,在酸性条件下铜和NO3-之间发生的氧化还原反应,即一定含有NO3-;
A.②加BaCl2出现白色沉淀;说明含有硫酸根离子,浓缩后加浓H2SO4和铜片共热产生红棕色气体NO2,一定含有NO3-,可能存在Na+,故A正确;
B.酸性溶液一定含有氢离子,这说明一定不含有CO32-,故B错误;
C.酸性溶液一定含有氢离子,这说明一定不含有SO32-,故C错误;
D.酸性溶液中硝酸根离子具有氧化性,亚硫酸根离子具有还原性,两者之间能发生的氧化还原反应不能共存,故D错误;
故选A.
点评 本题考查离子共存和离子检验的有关判断,题目难度中等,该题是高考中的常见题型,试题综合性强,旨在培养学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和规范的实验设计能力,注意干扰离子.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
10.常温下溶液pH小于7的是( )
| A. | 氯化钠溶液 | B. | 碳酸钠溶液 | C. | 醋酸溶液 | D. | 氢氧化钾溶液 |
11.丁烷受热分解可生成CH4、C2H6、C2H4、C3H6四者的混合气体,该混合气体的平均相对分子质量为( )
| A. | 58 | B. | 29 | C. | 14.5 | D. | 无法确定 |
15.现有7种物质:①乙烷;②乙烯;③乙炔;④苯;⑤甲苯;⑥溴乙烷;⑦聚丙烯.其中既能使酸性KMnO4 溶液褪色,又能与溴水反应使溴水褪色的是( )
| A. | ②③ | B. | ④⑥⑦ | C. | ①④⑥⑦ | D. | ②③⑤⑦ |
12.1mol乙醇与一定量的钠刚好完全反应后,溶液增加的质量( )
| A. | 11g | B. | 17g | C. | 44g | D. | 22g |
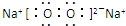 写出B的氢化物的结构式:
写出B的氢化物的结构式: 用电子式表示A、C两元素形成AC2的过程:
用电子式表示A、C两元素形成AC2的过程: