题目内容
4.配制100ml 0.1mol/L Na2CO3溶液,下列操作正确的是( )| A. | 称取1.06 g 无水碳酸钠,加入100ml容量瓶中,加水溶解、定容 | |
| B. | 称取1.06 g 无水碳酸钠,加入100ml蒸馏水,搅拌、溶解 | |
| C. | 转移Na2CO3溶液时,未用玻璃棒个引流,直接倒入容量瓶中 | |
| D. | 定容后,塞好瓶塞,反复倒转,摇匀 |
分析 配制100ml 0.1mol/L Na2CO3溶液,应称取碳酸钠的质量为0.1mol/L×0.1L×106g/mol=1.06g,即1.1g,溶于水配成溶液的体积为100ml,据此解答.
解答 解:A.配制溶液时,固体的溶解要在烧杯中进行,容量瓶是精密仪器,不能用容量瓶溶解,故A错误;
B.配制溶液时,体积指的是溶液体积,不是溶剂体积,不是加入100 mL蒸馏水,而是配制成100mL溶液,故B错误;
C.移液时未用玻璃棒引流,液体溅出,导致浓度偏小,故C错误;
D.定容后,塞好瓶塞,反复倒转,摇匀,使溶液均匀,故D正确;
故选:D.
点评 本题考查了配制一定物质的量浓度的溶液方法及误差分析,熟悉配制原理及实验操作步骤是解题关键,题目难度不大.

练习册系列答案
相关题目
12.下列实验操作中,正确的是( )
| A. | 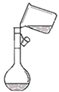 定容 | B. | 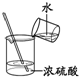 稀释浓硫酸 | C. | 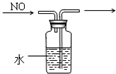 排水法收集NO | D. | 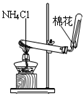 实验室制氨气 |
19.下列各组物质中,属于同系物的是( )
| A. | 苯和丙苯 | B. | 乙苯和间二甲苯 | C. | 丁二烯和丁烯 | D. | 萘和苯 |
13.下列分子或离子中,中心原子含有孤对电子的是( )
| A. | CH3+ | B. | CH3- | C. | SO42- | D. | NO3- |
14.酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是有碳粉,二氧化锰,氯化锌和氯化铵等组成的填充物,该电池在放电过程产生MnOOH,回收处理该废电池可以得到多种化工原料,有关数据下图所示:
溶解度/(g/100g水)
回下列问题:
(1)该电池的正极反应式为MnO2+H++e-=MnOOH,电池反应的离子方程式为2MnO2+Zn+2H+=2MnOOH+Zn2+
(2)每转移0.04mol电子,理论消耗Zn1.3g.(Zn的摩尔质量=65g/mol)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有氯化锌和氯化铵,两者可以通过加热浓缩、冷却结晶分离回收,滤渣的主要成分是二氧化锰、碳粉和MnOOH,欲从中得到较纯的二氧化锰,最简便的方法是空气中加热,其原理是碳粉转变为二氧化碳,MnOOH氧化为二氧化锰.
(4)用废电池的锌皮制作七水合硫酸锌,需去除少量杂质铁,其方法是:加入稀硫酸和双氧水,溶解,铁变为Fe3+,加碱调节PH为2.7,铁刚好完全沉淀(离子浓度小于1×10-5mol/L时,即可认为该离子沉淀完全).继续加碱调节PH为6,锌开始沉淀(假定Zn2+浓度为0.1mol/L).若上述过程不加双氧水的后果是Zn2+和Fe2+分离不开,原因是Zn(OH)2、Fe(OH)2的Ksp相近.
溶解度/(g/100g水)
| 温度0C化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
| NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
(1)该电池的正极反应式为MnO2+H++e-=MnOOH,电池反应的离子方程式为2MnO2+Zn+2H+=2MnOOH+Zn2+
(2)每转移0.04mol电子,理论消耗Zn1.3g.(Zn的摩尔质量=65g/mol)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有氯化锌和氯化铵,两者可以通过加热浓缩、冷却结晶分离回收,滤渣的主要成分是二氧化锰、碳粉和MnOOH,欲从中得到较纯的二氧化锰,最简便的方法是空气中加热,其原理是碳粉转变为二氧化碳,MnOOH氧化为二氧化锰.
(4)用废电池的锌皮制作七水合硫酸锌,需去除少量杂质铁,其方法是:加入稀硫酸和双氧水,溶解,铁变为Fe3+,加碱调节PH为2.7,铁刚好完全沉淀(离子浓度小于1×10-5mol/L时,即可认为该离子沉淀完全).继续加碱调节PH为6,锌开始沉淀(假定Zn2+浓度为0.1mol/L).若上述过程不加双氧水的后果是Zn2+和Fe2+分离不开,原因是Zn(OH)2、Fe(OH)2的Ksp相近.