题目内容
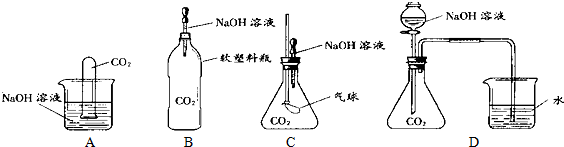
为探究CO2和NaOH确实发生了化学反应,某实验小组的同学设计了下列4种实验装置,请回答下列问题:

 (1)选择实验装置(3),简述出现的实验现象以及产生该实验现象的原因:____________。
(1)选择实验装置(3),简述出现的实验现象以及产生该实验现象的原因:____________。
(2)某同学质疑上述所有实验设计,该同学质疑的依据是______________________。
(3)在原实验的基础(4)上,请你设计实验证明CO2和NaOH肯定发生了化学反应。_______ ______________________________(用化学方程式表示即可)。
(1)气球变大;CO2与NaOH反应,使试管内压强减小。
(2)上述四种装置只能说明CO2减少,也可能是CO2溶解于水所致,并不能说明CO2一定和NaOH反应。
(3)点拨:取上述实验后的液体,滴加CaCl2溶液,若出现白色沉淀,说明原实验中CO2和NaOH反应生成了CO32-。即CaCl2 + Na2CO3 = CaCO3↓+ 2NaCl 或取上述实验后的溶液,滴加盐酸,看是否有气泡产生。Na2CO3+2HCl=2NaCl+H2O+CO2↑

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目