��Ŀ����
�ϳɰ���Ӧ��һ�����淴Ӧ��N2��g��+H2��g��?2NH3��g������298Kʱ����H=-92.2kJ?mol-1����S=-198.2J?K-1?mol-1��K=6.6��105Pa-2���ø�����ķ�ѹ��ʾ��ƽ�ⳣ�����������¶ȶԡ�H�͡�S��Ӱ�죬298K��1.01��105kPa�£��ں�ѹ���ܱ������г���10mol������30mol������20mol��������ʼ��˲�䣬��Ӧ�� ������У���Ӧһ��ʱ�����ϵ�����ı仯Ϊ ������ա��ų�����184.4kJ�������������Ϊԭ���� ����t minʱ��Ӧ�����Ӧ������У���Ӧ��Ϊ����������Ӧ������У���Ӧ��Ϊ������ת����Ϊ ��
���㣺��ѧƽ���Ӱ������,��ѧƽ��ļ���
ר�⣺��ѧƽ��ר��
����������ķ�ѹ֮�ȵ������ʵ���֮�ȣ����ݷ�Ӧ����ʽ�������ѹ֮�̣�Ȼ����ƽ�ⳣ���Ƚϣ��Ӷ����ж�ƽ���ƶ��������ƶ������жϷ�Ӧ�������仯�����ݷ�Ӧ������������ʵ��������ʱ�����ݻ�֮�ȣ����ݷ�Ӧ���ĵĵ��������ʵ�������Ӧǰ�����������ʵ��������������ת���ʣ�
���
�⣺����ķ�ѹ����������ʵ��������ȣ���Ӧ�տ�ʼʱ���������뷴Ӧ��ķ�ѹ��Ϊ��Q=
=
��K�����Է�Ӧ��������У�
���ڸ÷�Ӧ���ʱ��H��0����Ӧһ��ʱ�����ϵ�����ı仯Ϊ�ų�184.4kJ��
���������Ϣ��֪��ÿ�ų�92.2kJ������Ҫ��Ӧ��1mol��N2�����Էų�184.4kJ�������ĵĵ��������ʵ���Ϊ��
=2mol��
��ʱ��Ӧ��ϵ��N2ʣ������ʵ���Ϊ��10mol-2mol=8mol��H2ʣ�����ʵ���Ϊ��30mol-2mol��3=24mol�����ɵ�NH3�����ʵ���Ϊ4mol��
��tminʱ����������ʵ���Ϊ��8mol+24mol+24mol=56mol��
����tmin������������Ϊԭ���ģ�
=
��
������ת����Ϊ��
��100%=20%��
�ʴ�Ϊ������Ӧ���ų���
��20%��
| 202 |
| 101��303 |
| 4 |
| 2700 |
���ڸ÷�Ӧ���ʱ��H��0����Ӧһ��ʱ�����ϵ�����ı仯Ϊ�ų�184.4kJ��
���������Ϣ��֪��ÿ�ų�92.2kJ������Ҫ��Ӧ��1mol��N2�����Էų�184.4kJ�������ĵĵ��������ʵ���Ϊ��
| 184.4kJ |
| 92.2kJ/mol |
��ʱ��Ӧ��ϵ��N2ʣ������ʵ���Ϊ��10mol-2mol=8mol��H2ʣ�����ʵ���Ϊ��30mol-2mol��3=24mol�����ɵ�NH3�����ʵ���Ϊ4mol��
��tminʱ����������ʵ���Ϊ��8mol+24mol+24mol=56mol��
����tmin������������Ϊԭ���ģ�
| 56mol |
| 60mol |
| 14 |
| 15 |
������ת����Ϊ��
| 2mol |
| 10mol |
�ʴ�Ϊ������Ӧ���ų���
| 14 |
| 15 |
���������⿼���˻�ѧ��Ӧ�������仯����ѧƽ���Ӱ�����ء���ѧƽ�ⳣ���ļ��㣬��Ŀ�Ѷ��еȣ�ע�����ջ�ѧƽ�⼰��Ӱ�����أ���ȷ��ѧƽ�ⳣ���ĺ��弰���㷽��������������ѧ���ķ������������������Ӧ����ѧ֪ʶ��������

��ϰ��ϵ�д�
�����Ŀ
����˵����ȷ���ǣ�������
| A��HNO3��Ħ������Ϊ63 |
| B��Ħ�������ʵ����ĵ�λ |
| C��1mol�κ����ʶ�Լ����6.02��1023��ԭ�� |
| D��64g SO2���1mol O2 |
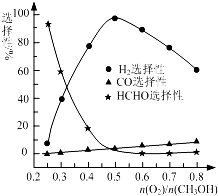 �״���Դ�ḻ���۸�������������淽�㣬������Ҫ����;��Ӧ��ǰ����
�״���Դ�ḻ���۸�������������淽�㣬������Ҫ����;��Ӧ��ǰ����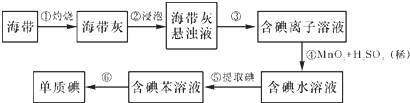
 ����ֲ���纣���������к��зḻ�ĵ�Ԫ�أ���Ԫ���Ե����ӵ���ʽ���ڣ�ʵ������Ӻ�������ȡ����������£�
����ֲ���纣���������к��зḻ�ĵ�Ԫ�أ���Ԫ���Ե����ӵ���ʽ���ڣ�ʵ������Ӻ�������ȡ����������£�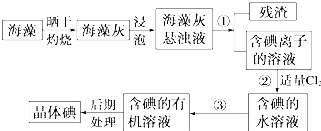
 X��Y��Z��W����ͼ��ʾ��ת����ϵ����X��Y��Z������
X��Y��Z��W����ͼ��ʾ��ת����ϵ����X��Y��Z������